العدد الذري للصوديوم: 11 | خصائصه واستخداماته
- ما هو العدد الذري للصوديوم؟
- ما هي أبرز خصائص عنصر الصوديوم؟
- 1. الخصائص الفيزيائية: معدن ناعم وخفيف
- 2. الخصائص الكيميائية: نشاط استثنائي
- ما هي أهم استخدامات الصوديوم؟
- 1. الصوديوم الفلزي: في الصناعات المتخصصة
- 2. مركبات الصوديوم: حيث تكمن الأهمية الكبرى
- من أين يأتي الصوديوم وكيف يُستخرج؟
- كيف تم اكتشاف الصوديوم؟
- المصادر والمراجع
- أسئلة شائعة حول العدد الذري للصوديوم وعنصره
- لماذا رمز الصوديوم Na وليس So؟
- ما الفرق بين الصوديوم والصودا؟
- هل الصوديوم ضروري للإنسان؟
- لماذا لا نستطيع لمس الصوديوم باليد؟
عندما نذكر ملح الطعام أو أضواء الشوارع الصفراء، فإننا نتحدث عن عنصر واحد: الصوديوم. لكن هل تساءلت يومًا ما الذي يحدد هوية هذا العنصر؟ الإجابة تكمن في رقم بسيط لكنه حاسم: العدد الذري للصوديوم. في هذا الدليل، سأأخذك في رحلة لفهم هذا العنصر الرائع، بدءًا من رقمه الذري وصولاً إلى استخداماته المذهلة في حياتنا اليومية.
ما هو العدد الذري للصوديوم؟
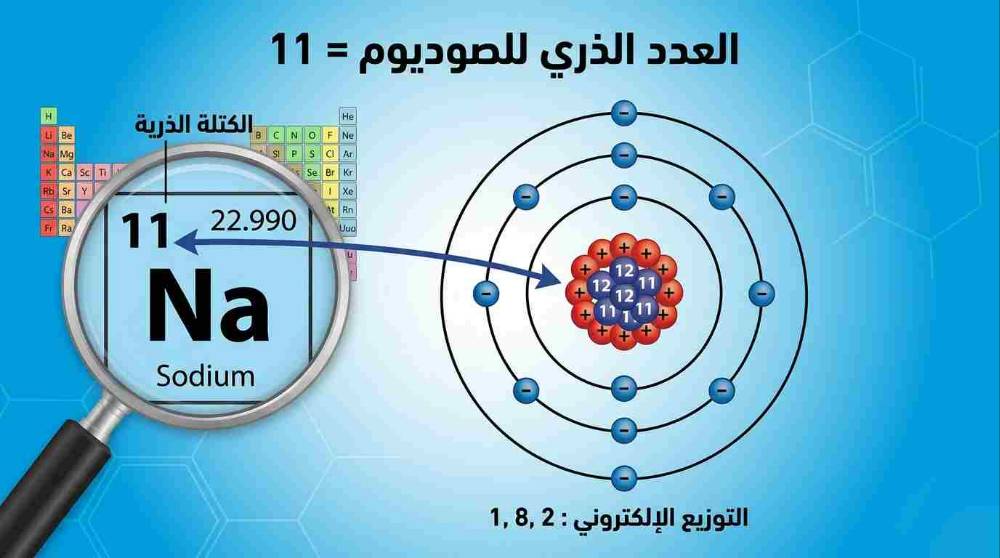
العدد الذري للصوديوم هو 11. هذا الرقم يعني أن نواة ذرة الصوديوم تحتوي على 11 بروتونًا. في الذرة المتعادلة كهربائيًا، يكون عدد الإلكترونات مساويًا لعدد البروتونات، أي 11 إلكترونًا أيضًا. هذا الرقم هو بطاقة هوية الصوديوم في الجدول الدوري، وهو الذي يحدد موقعه في المجموعة الأولى (الفلزات القلوية) والدورة الثالثة.
ما هي أبرز خصائص عنصر الصوديوم؟
بعد أن عرفنا أن العدد الذري للصوديوم هو 11، دعنا نتعرف على الخصائص التي تمنحها له هذه الذرات.
1. الخصائص الفيزيائية: معدن ناعم وخفيف
الصوديوم معدن ناعم جدًا لدرجة أنه يمكن قطعه بالسكين. كثافته منخفضة (0.97 جرام/سم³)، مما يجعله يطفو على سطح الماء. لونه أبيض فضي، لكنه يفقد لمعانه بسرعة فور تعرضه للهواء بسبب تكوين طبقة من الأكسيد. نقطة انصهاره منخفضة نسبيًا (97.8 درجة مئوية)، وهي أقل من درجة غليان الماء!
2. الخصائص الكيميائية: نشاط استثنائي
الصوديوم من أكثر العناصر نشاطًا كيميائيًا. يتفاعل بعنف مع الماء منتجًا هيدروكسيد الصوديوم وغاز الهيدروجين، وقد يشتعل الهيدروجين الناتج تلقائيًا بسبب حرارة التفاعل. لهذا السبب، يُحفظ الصوديوم تحت سطح الكيروسين أو الزيوت المعدنية، بعيدًا عن الرطوبة والهواء. كما يتفاعل بسرعة مع الأكسجين والكلور والعديد من العناصر الأخرى.
ما هي أهم استخدامات الصوديوم؟
على الرغم من نشاطه الكبير، فإن الصوديوم ومركباته تدخل في عدد لا يحصى من التطبيقات الحيوية والصناعية.
1. الصوديوم الفلزي: في الصناعات المتخصصة
على الرغم من ندرة استخدام الصوديوم في شكله الفلزي النقي مقارنة بمركباته، إلا له استخدامات حيوية:
- مبرد في المفاعلات النووية: يستخدم الصوديوم السائل كمبرد في بعض المفاعلات النووية السريعة لأنه لا يبطئ النيوترونات وله خواص حرارية ممتازة.
- صناعة التيتانيوم: يُستخدم الصوديوم في اختزال مركبات التيتانيوم لإنتاج المعدن النقي.
- مصابيح الإنارة: بخار الصوديوم هو المسؤول عن الضوء الأصفر المميز في أعمدة الإنارة، وهو يعطي كفاءة إضاءة عالية.
2. مركبات الصوديوم: حيث تكمن الأهمية الكبرى
الاستخدامات الحقيقية للصوديوم تأتي من مركباته المتنوعة:
- كلوريد الصوديوم (NaCl – ملح الطعام): يستخدم كتوابل أساسية في الطعام، وحافظ للمواد الغذائية، وفي إنتاج الكلور والصوديوم بالتحليل الكهربائي.
- هيدروكسيد الصوديوم (NaOH – الصودا الكاوية): يستخدم في صناعة الصابون والمنظفات، ومعالجة مياه الصرف، وتكرير النفط.
- كربونات الصوديوم (Na₂CO₃ – رماد الصودا): تدخل في صناعة الزجاج، ومنظفات الغسيل، وتنقية المياه.
- بيكربونات الصوديوم (NaHCO₃ – بيكربونات الصوديوم): تُستخدم في صناعة المخبوزات (بيكنج صودا)، ومضادات الحموضة، ومطفآت الحريق.
إذا كنت مهتمًا بشراء مركبات الصوديوم أو أي مواد كيميائية أخرى للاستخدامات الصناعية أو المختبرية، يمكنك زيارة متجر عالم الكيماويات للمواد الخام والكيماويات.
من أين يأتي الصوديوم وكيف يُستخرج؟
على الرغم من أن العدد الذري للصوديوم 11 يجعله أحد أكثر العناصر وفرة في القشرة الأرضية (سادس أكثر العناصر وفرة)، إلا أنه لا يوجد في الطبيعة بشكل حر بسبب نشاطه الكبير. يوجد الصوديوم في صورة مركبات، أهمها:
- الهاليت (الملح الصخري): كلوريد الصوديوم (NaCl)، وهو المصدر الرئيسي.
- الترونا (Trona): كربونات الصوديوم والبيكربونات.
- البوراكس (Borax): بورات الصوديوم.
- مياه البحر: تحتوي على كميات هائلة من كلوريد الصوديوم (حوالي 1.05%).
يتم استخلاص الصوديوم الفلزي تجاريًا عن طريق التحليل الكهربائي لكلوريد الصوديوم المنصهر عند درجة حرارة عالية، وليس من محاليله المائية، لأن الماء سيتفاعل مع الصوديوم المتكون. أما ملح الطعام، فيُستخرج من المناجم أو من تبخير مياه البحر.
كيف تم اكتشاف الصوديوم؟
قصة اكتشاف الصوديوم مثيرة وتعكس تطور الكيمياء الحديثة. رغم أن مركبات الصوديوم مثل الملح والصودا كانت معروفة منذ آلاف السنين (استخدمها قدماء المصريين في التحنيط وصناعة الزجاج)، إلا أن العنصر نفسه لم يُعزل إلا في عام 1807.
كان الكيميائي الإنجليزي العظيم السير همفري ديفي (Humphry Davy) هو أول من عزل الصوديوم. استخدم ديفي تقنية التحليل الكهربائي، حيث مرر تيارًا كهربائيًا قويًا عبر هيدروكسيد الصوديوم المنصهر (الصودا الكاوية)، فحصل على كريات صغيرة من معدن جديد. أطلق عليه اسم “صوديوم” (Sodium) اشتقاقًا من كلمة “صودا” (Soda). الرمز الكيميائي Na يأتي من الاسم اللاتيني “Natrium”، وهو مشتق من كلمة “نطرون” (Natron) التي كانت تستخدم لوصف الصودا في مصر القديمة.
المصادر والمراجع
اعتمدت في هذا الدليل على مصادر علمية موثوقة لضمان دقة المعلومات:
- Royal Society of Chemistry (RSC) – “Sodium – Element information, properties and uses” – تاريخ الاطلاع: مارس 2026 – https://www.rsc.org/periodic-table/element/11/sodium
- Encyclopaedia Britannica – “Sodium: Chemical properties” – خصائص الصوديوم وتفاعلاته – تاريخ الاطلاع: مارس 2026 – https://www.britannica.com/science/sodium/Chemical-properties
- Lenntech – “Sodium (Na) – Chemical properties, Health and Environmental effects” – تاريخ الاطلاع: مارس 2026 – https://www.lenntech.com/periodic/elements/na.htm
- PubChem – “Sodium | Na (Element)” – بيانات شاملة عن الخواص والنظائر والاستخدامات – تاريخ الاطلاع: مارس 2026 – https://pubchem.ncbi.nlm.nih.gov/element/Sodium
أسئلة شائعة حول العدد الذري للصوديوم وعنصره
لماذا رمز الصوديوم Na وليس So؟
يأتي الرمز Na من الاسم اللاتيني للعنصر “Natrium”، وهو مشتق من كلمة “نطرون” (Natron) التي كانت تستخدم في مصر القديمة لوصف كربونات الصوديوم. بينما يأتي الاسم الإنجليزي Sodium من كلمة “صودا” (Soda).
ما الفرق بين الصوديوم والصودا؟
الصوديوم هو العنصر الكيميائي نفسه (Na). أما “الصودا” فهي اسم شائع لمركبات الصوديوم، مثل صودا الخبز (بيكربونات الصوديوم) أو الصودا الكاوية (هيدروكسيد الصوديوم). لا يجب الخلط بين العنصر النشط الخطير ومركباته المستقرة.
هل الصوديوم ضروري للإنسان؟
نعم، أيونات الصوديوم (Na⁺) ضرورية للحياة. تلعب دورًا حيويًا في نقل الإشارات العصبية، انقباض العضلات، والحفاظ على توازن السوائل في الجسم. يحتاج الإنسان العادي إلى حوالي 2-3 جرام من الصوديوم يوميًا (على شكل ملح). لكن الإفراط في تناوله يرتبط بارتفاع ضغط الدم.
لماذا لا نستطيع لمس الصوديوم باليد؟
لأن الصوديوم الفلزي يتفاعل بعنف مع الرطوبة الموجودة على الجلد (الماء والعرق)، منتجًا هيدروكسيد الصوديوم (الصودا الكاوية) الذي يسبب حروقًا كيميائية عميقة. بالإضافة إلى أن التفاعل يطلق حرارة شديدة وقد يسبب اشتعال الهيدروجين الناتج.




💬 التعليقات