أنواع الروابط التساهمية
- ما هي الرابطة التساهمية ؟
- أنواع الروابط التساهمية من حيث عدد الإلكترونات المشتركة
- أولاً: الرابطة التساهمية الأحادية (Single Covalent Bond)
- ثانياً: الرابطة التساهمية الثنائية (Double Covalent Bond)
- ثالثاً: الرابطة التساهمية الثلاثية (Triple Covalent Bond)
- جدول مقارنة: أحادية، ثنائية، ثلاثية
- أنواع الروابط التساهمية من حيث قطبية الرابطة
- أولاً: الرابطة التساهمية غير القطبية (Nonpolar Covalent Bond)
- ثانياً: الرابطة التساهمية القطبية (Polar Covalent Bond)
- أنواع الروابط الكيميائية القوية (نظرة عامة)
- الأسئلة الشائعة
- ما الفرق بين الرابطة التساهمية القطبية وغير القطبية؟
- هل الرابطة الثنائية أقوى من الرابطة الأحادية؟
- هل يمكن لجزيء أن يحتوي على أكثر من رابطة تساهمية من أنواع مختلفة؟
- كيف أعرف إذا كانت الرابطة بين عنصرين تساهمية أم أيونية؟
- ما هي أقوى رابطة تساهمية معروفة؟
- المصادر والمراجع
ما هي الرابطة التساهمية ؟
الرابطة التساهمية (Covalent Bond) هي نوع من الروابط الكيميائية التي تنشأ عندما تشارك ذرتان أو أكثر بإلكترونات التكافؤ (الإلكترونات الموجودة في الغلاف الخارجي) بينهما. الهدف هو الوصول إلى حالة الاستقرار (قاعدة الثمانية – ثمانية إلكترونات في الغلاف الخارجي). تحدث الرابطة التساهمية عادة بين اللافلزات (مثل الهيدروجين والأكسجين والنيتروجين والكربون). قوة هذه الرابطة تأتي من تجاذب الإلكترونات المشتركة مع نواتي الذرتين معاً.
يشرح موقع Britannica أن الرابطة التساهمية هي أساس معظم الجزيئات العضوية واللاعضوية.
أنواع الروابط التساهمية من حيث عدد الإلكترونات المشتركة
يعتمد هذا التصنيف على عدد أزواج الإلكترونات التي تشترك فيها الذرتان:
أولاً: الرابطة التساهمية الأحادية (Single Covalent Bond)
تتشارك الذرتان بزوج واحد من الإلكترونات (إلكترونين). يُرمز لها بخط واحد (-). هي الأكثر شيوعاً وأطول وأضعف من الأنواع الأخرى. مثال: جزيء الهيدروجين (H-H) حيث تشترك ذرتا الهيدروجين بزوج إلكترون واحد. أيضاً الرابطة بين الكربون والهيدروجين في الميثان (CH₄).
ثانياً: الرابطة التساهمية الثنائية (Double Covalent Bond)
تتشارك الذرتان بزوجين من الإلكترونات (أربعة إلكترونات). تُرمز لها بخطين (=). أقصر وأقوى من الرابطة الأحادية. مثال: جزيء الأكسجين (O=O) حيث تشترك ذرتا الأكسجين بزوجين من الإلكترونات. أيضاً الرابطة بين ذرتي الكربون في الإيثيلين (C₂H₄).
ثالثاً: الرابطة التساهمية الثلاثية (Triple Covalent Bond)
تتشارك الذرتان بثلاثة أزواج من الإلكترونات (ستة إلكترونات). تُرمز لها بثلاثة خطوط (≡). الأقصر والأقوى بين الروابط التساهمية. مثال: جزيء النيتروجين (N≡N) حيث تشترك ذرتا النيتروجين بثلاثة أزواج من الإلكترونات. أيضاً الإيثاين (C₂H₂).
موقع LibreTexts يشرح هذه الأنواع بالتفصيل مع أمثلة.
جدول مقارنة: أحادية، ثنائية، ثلاثية
| نوع الرابطة | عدد أزواج الإلكترونات | الرمز | القوة النسبية | مثال |
|---|---|---|---|---|
| أحادية | 1 زوج (إلكترونين) | – | أضعف، أطول | H-H، Cl-Cl، CH₄ |
| ثنائية | 2 زوج (4 إلكترونات) | = | أقوى من الأحادية | O=O، C=C |
| ثلاثية | 3 أزواج (6 إلكترونات) | ≡ | الأقوى، الأقصر | N≡N، C≡C |
أنواع الروابط التساهمية من حيث قطبية الرابطة
تعتمد قطبية الرابطة على مدى تساوي مشاركة الإلكترونات بين الذرتين. إذا كان للذرتين نفس القدرة على جذب الإلكترونات (الكهرسلبية)، تكون المشاركة متساوية. وإلا، تكون غير متساوية.
أولاً: الرابطة التساهمية غير القطبية (Nonpolar Covalent Bond)
تحدث عندما تتشارك ذرتان متماثلتان (نفس العنصر) أو ذرتان لهما نفس الكهرسلبية تقريباً (فرق الكهرسلبية أقل من 0.4). توزيع الإلكترونات متساوٍ تماماً. أمثلة: H₂، Cl₂، O₂، N₂، CH₄ (على الرغم من اختلاف الذرات، لكن فرق الكهرسلبية صغير والهندسة الجزيئية تجعل الجزيء غير قطبي).
ثانياً: الرابطة التساهمية القطبية (Polar Covalent Bond)
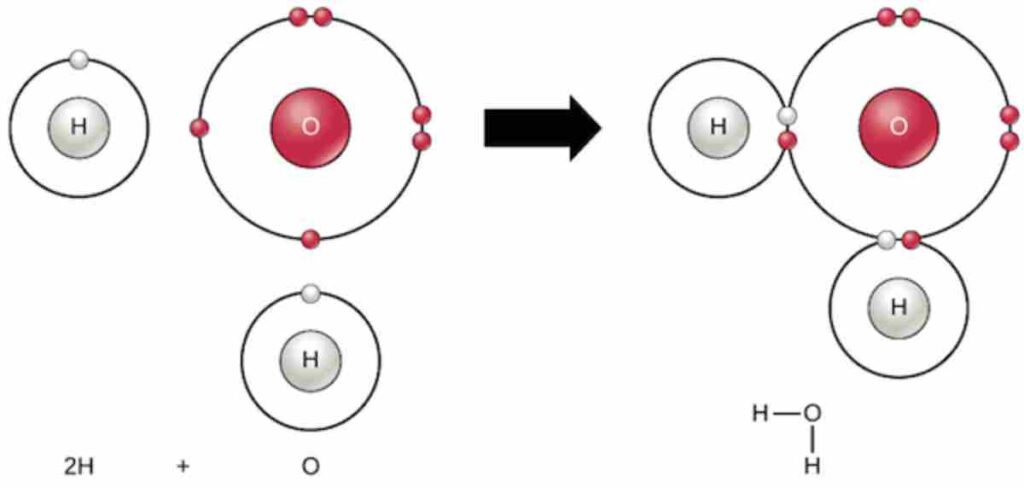
تحدث عندما تتشارك ذرتان مختلفتان في الكهرسلبية (فرق الكهرسلبية بين 0.4 و 1.7). الإلكترونات تنجذب أكثر نحو الذرة الأكثر كهرسلبية، فتكتسب شحنة سالبة جزئية (δ⁻)، بينما تكتسب الذرة الأخرى شحنة موجبة جزئية (δ⁺). هذا يخلق ثنائي قطب (Dipole). أشهر مثال: الماء (H₂O) حيث الأكسجين أكثر كهرسلبية من الهيدروجين، فتنجذب الإلكترونات نحو الأكسجين. أمثلة أخرى: HCl، NH₃.
قاعدة تذكير: الرابطة بين ذرتين متماثلتين = غير قطبية. الرابطة بين ذرتين مختلفتين (مثل H-Cl) = قطبية عادةً.
موقع LibreTexts يشرح قاعدة الثمانية التي تشرح سبب تكوين الذرات للروابط.
أنواع الروابط الكيميائية القوية (نظرة عامة)
ضمن سياق الروابط القوية (الروابط الأساسية التي تمسك الذرات معاً لتكوين الجزيئات أو البلورات)، هناك ثلاثة أنواع رئيسية. الرابطة التساهمية هي أحدها:
- الرابطة التساهمية (Covalent Bond): مشاركة إلكترونات بين اللافلزات (شرحناها بالتفصيل أعلاه).
- الرابطة الأيونية (Ionic Bond): انتقال كامل للإلكترونات من فلز إلى لافلز، فتتكون أيونات موجبة وسالبة تتجاذب كهربائياً. تحدث عادة بين الفلزات واللافلزات (مثل NaCl).
- الرابطة الفلزية (Metallic Bond): “بحر من الإلكترونات” تتحرك بحرية بين شبكة من أيونات الفلزات الموجبة. تحدث في المعادن النقية والسبائك (مثل النحاس والحديد).
الروابط التساهمية والأيونية والفلزية كلها روابط قوية (Primary Bonds). قوة الرابطة التساهمية تتراوح بين 50-1100 كيلوجول/مول. الرابطة الثلاثية هي الأقوى، ثم الثنائية، ثم الأحادية. موقع ZME Science يشرح أنواع الروابط الكيميائية القوية.
إذا كنت مهتماً بالروابط التي تؤدي لتكوين الأيونات، يمكنك قراءة مقالنا عن الأيون الموجب والسالب.
الأسئلة الشائعة
ما الفرق بين الرابطة التساهمية القطبية وغير القطبية؟
في غير القطبية، تتشارك الذرات الإلكترونات بالتساوي (لأنها متماثلة أو متساوية الكهرسلبية). في القطبية، تنجذب الإلكترونات نحو الذرة الأكثر كهرسلبية، فتتوزع بشكل غير متساوٍ.
هل الرابطة الثنائية أقوى من الرابطة الأحادية؟
نعم، الرابطة الثنائية أقوى وأقصر من الأحادية. والرابطة الثلاثية أقوى وأقصر من الثنائية. لكن الطاقة المطلوبة لكسر الرابطة الثلاثية ليست ثلاثة أضعاف الأحادية؛ لأن هناك تفاعلات إلكترونية معقدة.
هل يمكن لجزيء أن يحتوي على أكثر من رابطة تساهمية من أنواع مختلفة؟
نعم. مثال: جزيء الإيثيلين (C₂H₄) يحتوي على رابطة ثنائية بين ذرتي الكربون، وأربع روابط أحادية بين الكربون والهيدروجين. جزيء الإيثاين (C₂H₂) يحتوي على رابطة ثلاثية بين الكربونين ورابطتين أحاديتين.
كيف أعرف إذا كانت الرابطة بين عنصرين تساهمية أم أيونية؟
إذا كان الفرق في الكهرسلبية أكبر من 1.7، غالباً الرابطة أيونية. إذا كان أقل من 1.7، غالباً تساهمية (وإذا كان أقل من 0.4، غير قطبية). هذا المقياس ليس حاسماً بنسبة 100% لكنه دليل جيد.
ما هي أقوى رابطة تساهمية معروفة؟
الرابطة بين الكربون والنيتروجين (C≡N) في النتريلات، أو الرابطة بين النيتروجين نفسه (N≡N) في غاز النيتروجين، تعتبر من أقوى الروابط التساهمية (طاقة تفكك حوالي 945 كيلوجول/مول).




💬 التعليقات