ما هو العدد الذري للعناصر
- العدد الذري للعناصر: فهم هوية المادة وترتيب الجدول الدوري
- هوية العنصر: لماذا البروتونات هي المفتاح؟
- الترتيب في الجدول الدوري: ثورة موزلي
- الفرق بين العدد الذري والعدد الكتلي
- كيف يتحكم العدد الذري في خصائص المادة؟
- الخلاصة: الرقم الذي يحكم المادة
- أسئلة شائعة حول العدد الذري للعناصر
- هل يمكن لعنصرين مختلفين امتلاك نفس العدد الذري؟
- أين يكتب العدد الذري في رمز العنصر؟
- ما هو أكبر عدد ذري مكتشف حتى الآن؟
العدد الذري للعناصر: فهم هوية المادة وترتيب الجدول الدوري
يُعد العدد الذري للعناصر هو البصمة الوراثية الحقيقية لكل مادة في هذا الكون، حيث يمثل الرقم الفريد الذي لا يتكرر بين عنصرين أبداً. فـ العدد الذري للعناصر (Atomic Number) هو عدد البروتونات الموجودة في نواة ذرة العنصر، ويرمز له عالمياً بالرمز Z. إن فهم العدد الذري للعناصر هو حجر الزاوية في الكيمياء الحديثة؛ فهو الذي يحدد موقع العنصر في الجدول الدوري، ويتحكم في خصائصه الكيميائية، وطريقة تفاعله مع العناصر الأخرى. بدون هذا الرقم، لكانت الكيمياء مجرد فوضى من المواد المجهولة، ولكن بفضله استطعنا تنظيم الكون المادي في نظام دقيق ومبهر.
هوية العنصر: لماذا البروتونات هي المفتاح؟
“العدد الذري هو الذي يحدد نوع العنصر؛ فإذا تغير عدد البروتونات في النواة، يتغير العنصر تماماً ويتحول إلى مادة أخرى مختلفة كلياً في خصائصها.”
عند دراسة العدد الذري للعناصر، نجد أن ذرة الهيدروجين تمتلك بروتوناً واحداً (Z=1)، بينما يمتلك الذهب 79 بروتوناً (Z=79). للمزيد حول المواد والتركيبات الكيميائية، يمكنك زيارة موقع المواد الكيميائية المتخصص. من المهم ملاحظة أن العدد الذري يساوي أيضاً عدد الإلكترونات في الذرة المتعادلة كهربائياً، وهو ما يحدد التوزيع الإلكتروني وبالتالي السلوك الكيميائي للعنصر في التفاعلات المختلفة.
الترتيب في الجدول الدوري: ثورة موزلي
تاريخياً، كان العلماء يرتبون العناصر حسب كتلتها الذرية، ولكن اكتشاف العدد الذري للعناصر أحدث ثورة بقيادة العالم هنري موزلي.
- التسلسل المنطقي: تُرتب العناصر في الجدول الدوري الحديث تصاعدياً حسب أعدادها الذرية، مما حل التناقضات التي ظهرت في الجداول القديمة.
- الدورات والمجموعات: يؤدي التزايد المنتظم في
Atomic Numberإلى تكرار الخصائص الكيميائية بشكل دوري، مما يسمح بتصنيف العناصر في مجموعات ذات صفات متشابهة. - العناصر المفقودة: ساعد فهم العدد الذري للعناصر العلماء على التنبؤ بوجود عناصر لم تكن مكتشفة بعد، وذلك بوجود فجوات في تسلسل الأرقام الذرية.
يمكنك الاطلاع على القائمة الكاملة للأرقام الذرية عبر ويكيبيديا: قائمة العناصر الكيميائية.
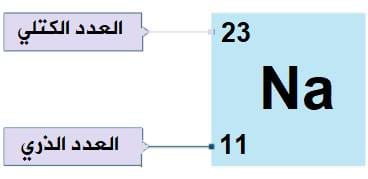
الفرق بين العدد الذري والعدد الكتلي
يخلط الكثيرون بين العدد الذري للعناصر والعدد الكتلي، ولكن الفرق جوهري:
- العدد الذري (Z): هو عدد البروتونات فقط، وهو ثابت لجميع ذرات العنصر الواحد.
- العدد الكتلي (A): هو مجموع عدد البروتونات والنيوترونات في النواة، وقد يختلف بين ذرات نفس العنصر فيما يعرف بـ النظائر (Isotopes).
تؤكد برنامج الأمم المتحدة للبيئة (UNEP) على أهمية مراقبة النظائر المشعة لبعض العناصر ذات الأعداد الذرية العالية في البيئة لضمان السلامة الإشعاعية وحماية التنوع البيولوجي.
كيف يتحكم العدد الذري في خصائص المادة؟
بما أن العدد الذري للعناصر يحدد عدد الإلكترونات، فإنه يتحكم بشكل مباشر في “إلكترونات التكافؤ” الموجودة في المدار الخارجي. هذه الإلكترونات هي المسؤولة عن الروابط الكيميائية؛ فمثلاً، العناصر التي تمتلك عدداً ذرياً يجعل مدارها الخارجي مكتملاً (مثل الغازات النبيلة) تكون خاملة جداً، بينما العناصر التي تحتاج لإلكترون واحد (مثل الهالوجينات) تكون شديدة التفاعل.
الخلاصة: الرقم الذي يحكم المادة
في الختام، يظل العدد الذري للعناصر هو المفتاح الذهبي لفهم لغة الكون الكيميائية. من الهيدروجين البسيط إلى الأوجانيسون المعقد، يخبرنا هذا الرقم بقصة كل ذرة ومكانها في نسيج الوجود. إن احترامنا لهذا الترتيب الدقيق مكننا من ابطكار مواد جديدة، وأدوية منقذة للحياة، وتقنيات طاقة متطورة. العدد الذري ليس مجرد رقم في كتاب مدرسي، بل هو القانون الذي يضمن استقرار وتنوع المادة التي تشكلنا وتشكل عالمنا.
| العنصر | الرمز | العدد الذري (Z) | الأهمية الحيوية/الصناعية |
|---|---|---|---|
| الهيدروجين | H | 1 | وقود النجوم والكون |
| الكربون | C | 6 | أساس الحياة العضوية |
| الأكسجين | O | 8 | ضروري للتنفس والاحتراق |
| اليورانيوم | U | 92 | مصدر للطاقة النووية |
أسئلة شائعة حول العدد الذري للعناصر
هل يمكن لعنصرين مختلفين امتلاك نفس العدد الذري؟
مستحيل؛ فـ العدد الذري للعناصر هو تعريف العنصر نفسه. إذا تساوى عدد البروتونات، فهما حتماً نفس العنصر، حتى لو اختلف عدد النيوترونات (النظائر).
أين يكتب العدد الذري في رمز العنصر؟
يُكتب العدد الذري عادة كـ “رقم سفلي” إلى يسار رمز العنصر (مثلاً 6C)، بينما يُكتب العدد الكتلي كـ “رقم علوي” (مثلاً 12C).
ما هو أكبر عدد ذري مكتشف حتى الآن؟
أكبر عدد ذري للعناصر معترف به رسمياً هو 118، وهو لعنصر “الأوجانيسون” (Oganesson)، وهو عنصر اصطناعي فائق الثقل تم تحضيره في المختبرات النووية.




💬 التعليقات