العدد الكتلي (A) : تعريفه ، حسابه
- ما هو العدد الكتلي؟
- كيف يتم حساب العدد الكتلي؟
- أمثلة على حساب العدد الكتلي
- ما الفرق بين العدد الكتلي والكتلة الذرية؟
- 1. التعريف والأساس
- 2. الاختلاف عن الكتلة الفعلية
- جدول مقارنة سريع
- ما هي العلاقة بين العدد الكتلي والنظائر؟
- المصادر والمراجع
- أسئلة شائعة حول العدد الكتلي
- ما الفرق بين العدد الكتلي والعدد الذري؟
- لماذا العدد الكتلي ليس هو نفس الكتلة الذرية في الجدول الدوري؟
- كيف أحسب عدد النيوترونات إذا كنت أعرف العدد الكتلي والعدد الذري؟
- هل العدد الكتلي للعنصر ثابت دائماً؟
عندما تنظر إلى الجدول الدوري، ترى أرقاماً معقدة تحت كل عنصر. لكن خلف هذه الأرقام تكمن قصة بسيطة عن مكونات الذرة. أحد أهم هذه الأرقام هو العدد الكتلي (Mass Number)، الذي يُعرف أيضاً بالعدد النووي أو عدد النكليونات. في هذا الدليل، سنتعرف على العدد الكتلي، وكيفية حسابه، والفرق بينه وبين الكتلة الذرية، ولماذا هو مفتاح لفهم النظائر المختلفة للعناصر.

ما هو العدد الكتلي؟
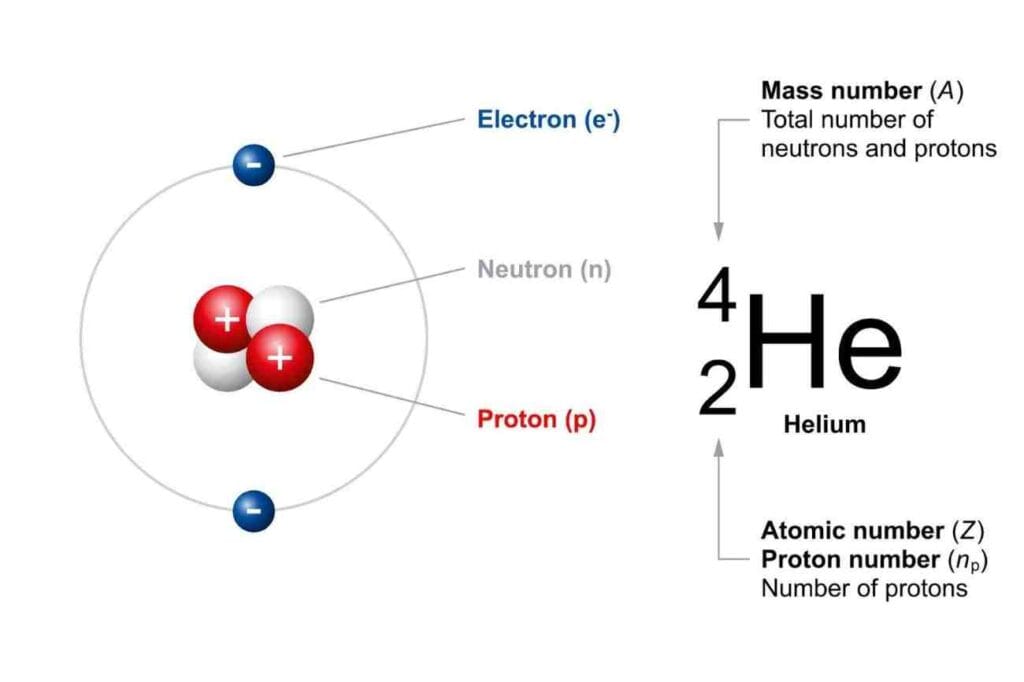
العدد الكتلي (Mass Number) ورمزه (A)، هو مجموع عدد البروتونات وعدد النيوترونات الموجودة في نواة الذرة. يُسمى أيضاً العدد النووي أو عدد النكليونات (Nucleon Number)، لأن البروتونات والنيوترونات تُسمى مجتمعة “نكليونات”. العدد الكتلي هو عدد صحيح (لأنه عدد من الجسيمات)، ويُكتب عادةً بخط صغير فوق رمز العنصر في الترميز النووي (مثل ¹²C للكربون-12).
كيف يتم حساب العدد الكتلي؟
حساب العدد الكتلي بسيط للغاية. يكفي معرفة عدد البروتونات (العدد الذري Z) وعدد النيوترونات (N) في نواة الذرة. العلاقة هي:
العدد الكتلي (A) = عدد البروتونات (Z) + عدد النيوترونات (N)
نظراً لأن الإلكترونات كتلتها ضئيلة جداً (حوالي 1/1836 من كتلة البروتون)، فإنها لا تُضاف إلى العدد الكتلي. يعطي العدد الكتلي تقريباً لكتلة النواة بوحدة الكتل الذرية (amu).
أمثلة على حساب العدد الكتلي
- الكربون-12 (¹²C): يحتوي على 6 بروتونات و 6 نيوترونات، لذا العدد الكتلي = 6 + 6 = 12.
- اليورانيوم-238 (²³⁸U): يحتوي على 92 بروتوناً و 146 نيوتروناً، لذا العدد الكتلي = 92 + 146 = 238.
- الهيدروجين-1 (¹H): يحتوي على بروتون واحد ولا يحتوي على نيوترونات، لذا العدد الكتلي = 1 + 0 = 1.
ما الفرق بين العدد الكتلي والكتلة الذرية؟
هذا من أكثر الأسئلة شيوعاً في الكيمياء. هناك فرق جوهري بين العدد الكتلي والكتلة الذرية (Atomic Mass)، وهو:
1. التعريف والأساس
- العدد الكتلي (A): هو عدد صحيح يمثل عدد البروتونات والنيوترونات في نواة ذرة معينة (نظير محدد). وهو قيمة محسوبة وليست مقاسة تجريبياً.
- الكتلة الذرية: هي متوسط كتل جميع النظائر الطبيعية للعنصر، مرجحة بنسبة تواجدها في الطبيعة. غالباً ما تكون قيمة عشرية لأنها تعكس وجود نظائر مختلفة. تُقاس بالوحدة الذرية (amu). على سبيل المثال، الكلور له عدد كتلي 35 و 37 لنظائره، لكن كتلته الذرية هي 35.45 amu.
2. الاختلاف عن الكتلة الفعلية
حتى بالنسبة لنظير واحد، فإن الكتلة الفعلية للنواة بالوحدة الذرية (amu) لا تساوي العدد الكتلي بالضبط. هذا بسبب ظاهرة تسمى نقص الكتلة (Mass Defect). عندما تتحد البروتونات والنيوترونات لتكوين النواة، يتحول جزء صغير من كتلتها إلى طاقة (حسب معادلة أينشتاين E=mc²). هذه الطاقة هي طاقة الربط النووي (Binding Energy). لذلك، الكتلة الفعلية للنواة تكون دائماً أقل بقليل من مجموع كتل البروتونات والنيوترونات المنفردة. للمزيد حول طاقة الربط النووي، يمكنك الاطلاع على مقالنا عن التفاعلات النووية.
جدول مقارنة سريع
| الخاصية | العدد الكتلي (A) | الكتلة الذرية |
|---|---|---|
| التعريف | عدد البروتونات + النيوترونات | متوسط كتل النظائر (بالوحدة الذرية) |
| القيمة | عدد صحيح | عدد عشري غالباً |
| ما يمثله | نظير محدد | متوسط العنصر (جميع نظائره) |
| أين يوجد؟ | فوق رمز العنصر (في الترميز النووي) | أسفل رمز العنصر في الجدول الدوري |
ما هي العلاقة بين العدد الكتلي والنظائر؟
النظائر (Isotopes) هي ذرات لنفس العنصر (نفس العدد الذري Z) ولكنها تختلف في عدد النيوترونات، وبالتالي تختلف في العدد الكتلي (A). مثلاً، الكربون له ثلاثة نظائر طبيعية:
- الكربون-12 (¹²C): 6 بروتونات + 6 نيوترونات → A = 12.
- الكربون-13 (¹³C): 6 بروتونات + 7 نيوترونات → A = 13.
- الكربون-14 (¹⁴C): 6 بروتونات + 8 نيوترونات → A = 14.
لاحظ أن العدد الذري (Z) ثابت لجميع النظائر (6 للكربون)، أما العدد الكتلي (A) فيختلف باختلاف النظير. هذا المفهوم أساسي في الكيمياء النووية والعديد من التطبيقات العلمية.
إذا كنت مهتماً بشراء مواد الكيمياء عالية الجودة ، يمكنك زيارة متجر عالم الكيماويات للمواد الخام والكيماويات حيث نوفر مجموعة واسعة من المواد الكيميائية عالية النقاء.
المصادر والمراجع
اعتمدت في هذا الدليل على مصادر علمية موثوقة:
- Encyclopaedia Britannica – “Mass number” – تاريخ الاطلاع: أبريل 2026 – https://www.britannica.com/science/mass-number
- Energy Education – “Mass number” – تاريخ الاطلاع: أبريل 2026 – https://energyeducation.ca/encyclopedia/Mass_number
- Lumen Learning – “Atomic Number and Mass Number” – تاريخ الاطلاع: أبريل 2026 – https://courses.lumenlearning.com/introchem/chapter/atomic-number-and-mass-number/
- Byju’s – “Atomic Number and Mass Number” – تاريخ الاطلاع: أبريل 2026 – https://byjus.com/chemistry/atomic-number-mass-number/
- Aus-e-Tute – “Mass Number of an Atom Chemistry Tutorial” – تاريخ الاطلاع: أبريل 2026 – https://www.ausetute.com.au/massnumber.html
أسئلة شائعة حول العدد الكتلي
ما الفرق بين العدد الكتلي والعدد الذري؟
العدد الذري (Z) هو عدد البروتونات فقط، ويحدد هوية العنصر. أما العدد الكتلي (A) فهو مجموع البروتونات والنيوترونات، ويعطي كتلة النواة التقريبية. الفرق بين العدد الكتلي والعدد الذري (A – Z) يعطي عدد النيوترونات في النواة.
لماذا العدد الكتلي ليس هو نفس الكتلة الذرية في الجدول الدوري؟
لأن الكتلة الذرية في الجدول الدوري هي متوسط مرجح لكتل جميع النظائر الطبيعية للعنصر. معظم العناصر لها نظائر متعددة، لذا فإن متوسط كتلتها يكون عدداً عشرياً. أما العدد الكتلي فيشير إلى نظير محدد فقط، وهو عدد صحيح.
كيف أحسب عدد النيوترونات إذا كنت أعرف العدد الكتلي والعدد الذري؟
عدد النيوترونات = العدد الكتلي (A) – العدد الذري (Z). مثلاً، نظير الألومنيوم-27 (²⁷Al) له عدد ذري 27 (وهو 13)؟ العدد الذري للألومنيوم هو 13. إذاً عدد النيوترونات = 27 – 13 = 14 نيوتروناً.
هل العدد الكتلي للعنصر ثابت دائماً؟
لا، ليس ثابتاً. العنصر الواحد يمكن أن يكون له عدة نظائر، ولكل نظير عدد كتلي مختلف. الكلور، مثلاً، له نظيران رئيسيان: كلور-35 (A=35) وكلور-37 (A=37). العدد الذري ثابت (17)، لكن العدد الكتلي يختلف حسب النظير.




💬 التعليقات