ما هي الغازات النبيلة ؟ خصائصها واستخداماتها
- ما هي الغازات النبيلة؟
- ما هي عناصر مجموعة الغازات النبيلة؟
- 1. الهيليوم (Helium – He)
- 2. النيون (Neon – Ne)
- 3. الأرجون (Argon – Ar)
- 4. الكريبتون (Krypton – Kr)
- 5. الزينون (Xenon – Xe)
- 6. الرادون (Radon – Rn)
- 7. أوغانيسون (Oganesson – Og)
- ما هي الصفات المشتركة لجميع الغازات النبيلة؟
- 1. الخمول الكيميائي (الاستقرار الإلكتروني)
- 2. الخواص الفيزيائية المتدرجة
- 3. أحادية الذرة (Monatomic)
- 4. عدم التوصيل الكهربائي في الظروف العادية
- ما هي أهمية الغازات النبيلة في حياتنا اليومية؟
- المصادر والمراجع
- أسئلة شائعة حول الغازات النبيلة
- لماذا تسمى الغازات النبيلة بهذا الاسم؟
- هل يمكن للغازات النبيلة أن تشكل مركبات كيميائية؟
- ما هي الطريقة المتبعة لاستخلاص الغازات النبيلة من الهواء؟
- هل غاز الرادون خطير على الصحة؟
عندما ترى أضواء النيون المتوهجة في شوارع المدن الكبرى، أو تشاهد بالونات الهيليوم وهي ترتفع في الهواء، فإنك تتفاعل مع الغازات النبيلة. هذه المجموعة الفريدة من العناصر الكيميائية، التي تقع في أقصى يمين الجدول الدوري، كانت تُعرف سابقاً باسم “الغازات الخاملة” بسبب اعتقاد خاطئ بأنها لا تتفاعل مع أي شيء. لكن الواقع أكثر إثارة للاهتمام. في هذا الدليل الشامل، سأأخذك في رحلة لاستكشاف عالم الغازات النبيلة: ما هي، ومن أين أتت، وما الذي يجعلها مميزة، وكيف أصبحت جزءاً لا يتجزأ من حياتنا اليومية.
ما هي الغازات النبيلة؟
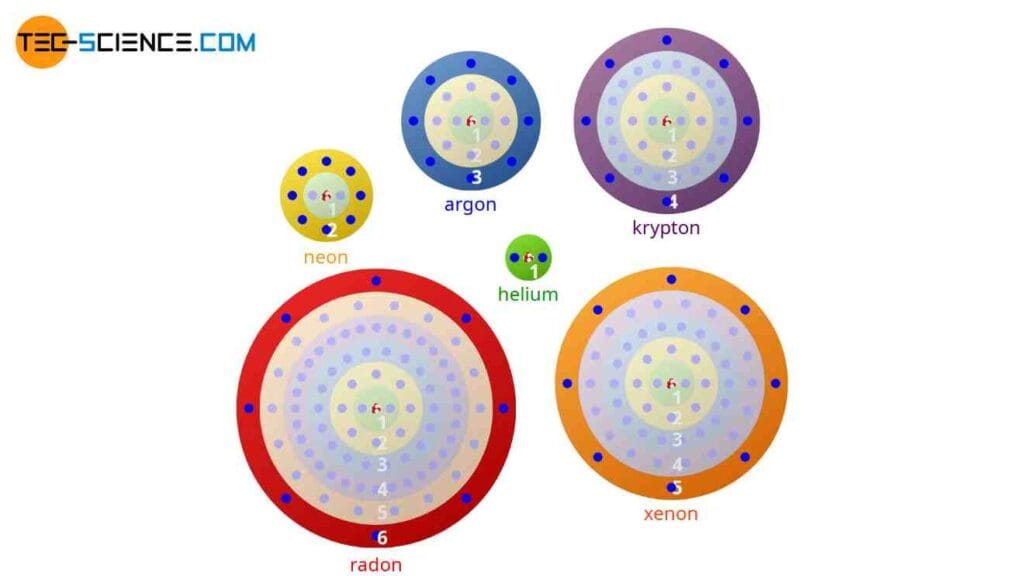
الغازات النبيلة هي العناصر الكيميائية التي تشكل المجموعة 18 (المجموعة VIII A سابقاً) في الجدول الدوري. تضم هذه المجموعة ستة غازات طبيعية: الهيليوم (He)، والنيون (Ne)، والأرجون (Ar)، والكريبتون (Kr)، والزينون (Xe)، والرادون (Rn)، بالإضافة إلى العنصر الاصطناعي أوغانيسون (Og). تتميز هذه العناصر بكونها غازات عديمة اللون والرائحة والطعم في الظروف العادية، وهي شديدة الخمول كيميائياً بسبب امتلاء غلافها الإلكتروني الخارجي بالكامل.
ما هي عناصر مجموعة الغازات النبيلة؟
تتكون مجموعة الغازات النبيلة من سبعة عناصر، ستة منها تتواجد طبيعياً في الغلاف الجوي للأرض بتراكيز متفاوتة. إليك قائمة بها مع نبذة سريعة عن كل منها:
1. الهيليوم (Helium – He)
الهيليوم هو ثاني أخف عنصر في الكون بعد الهيدروجين. اكتشف لأول مرة في الشمس قبل أن يعثر عليه على الأرض. يتميز بخفته الشديدة وعدم قابليته للاشتعال، مما يجعله الخيار الأمثل لملء بالونات الطقس والمناطيد. يستخدم أيضاً كمبرد فائق البرودة في أجهزة التصوير بالرنين المغناطيسي (MRI).
2. النيون (Neon – Ne)
النيون هو ملك إعلانات الليل. عند تمرير تيار كهربائي عبر أنبوب مملوء بالنيون، يتوهج بضوء أحمر برتقالي مميز. مع إضافة مواد أخرى، يمكن الحصول على ألوان متعددة. يستخدم النيون في لافتات الإعلانات المضيئة، ومصابيح التحذير، وفي أجهزة الليزر.
3. الأرجون (Argon – Ar)
الأرجون هو أكثر الغازات النبيلة وفرة في الغلاف الجوي للأرض، حيث يشكل حوالي 0.93% من الهواء. اكتشفه اللورد رايلي وويليام رامزي عام 1894. يُستخدم الأرجون على نطاق واسع كغاز خامل في لحام المعادن (لحماية منطقة اللحام من الأكسجين)، وفي إضاءة المصابيح الكهربائية، وفي صناعة أشباه الموصلات.
4. الكريبتون (Krypton – Kr)
يشتق اسم الكريبتون من الكلمة اليونانية “كريبتوس” (κρυπτός) التي تعني “المخفي”، وهو مناسب لأنه كان صعب الاكتشاف. يستخدم الكريبتون في مصابيح الفلورسنت عالية الكفاءة، وفي ومضات الكاميرات فائقة السرعة. بين عامي 1960 و1983، استخدم نظير الكريبتون-86 لتحديد طول المتر.
5. الزينون (Xenon – Xe)
الزينون، الذي يعني اسمه “الغريب”، كان أول غاز نبيل يُكتشف أنه يمكنه تكوين مركبات كيميائية حقيقية، مما قلب المفاهيم السائدة في الكيمياء. يستخدم الزينون في مصابيح الفلاش القوية (مثل الكاميرات)، وفي أضواء السيارات الأمامية (زينون HID)، وفي التخدير نظراً لخصائصه المخدرة الفريدة.
6. الرادون (Radon – Rn)
الرادون هو غاز نبيل مشع يتكون من التحلل الطبيعي للراديوم واليورانيوم في التربة والصخور. وهو أثقل الغازات النبيلة. الخطر الرئيسي للرادون هو أنه يمكن أن يتراكم في المنازل المغلقة، واستنشاقه يزيد من خطر الإصابة بسرطان الرئة. يُعد ثاني أكبر سبب لسرطان الرئة بعد التدخين.
7. أوغانيسون (Oganesson – Og)
العنصر السابع في المجموعة، وهو العنصر الأثقل في الجدول الدوري حتى الآن (العدد الذري 118). تم تصنيعه لأول مرة عام 2002 في روسيا. نظراً لعمره القصير جداً (أجزاء من الألف من الثانية)، فإن خواصه الكيميائية غير معروفة بعد، لكن من المتوقع أن تختلف عن بقية الغازات النبيلة بسبب التأثيرات النسبية.
ما هي الصفات المشتركة لجميع الغازات النبيلة؟
على الرغم من اختلاف أحجامها وكتلها الذرية، تشترك جميع الغازات النبيلة في مجموعة من الخصائص الفيزيائية والكيميائية الفريدة:
1. الخمول الكيميائي (الاستقرار الإلكتروني)
السبب الجذري لخمول الغازات النبيلة هو امتلاء مدارها الإلكتروني الخارجي بالكامل. فالهيليوم له مدار s مملوء (1s²)، وباقي العناصر لها تكوين إلكتروني ns² np⁶ (قاعدة الثمانية). هذا الترتيب مستقر للغاية، مما يجعلها لا تميل إلى فقد أو اكتساب أو مشاركة الإلكترونات مع العناصر الأخرى.
2. الخواص الفيزيائية المتدرجة
مع زيادة العدد الذري (من الهيليوم إلى الرادون)، تزداد كثافة الغازات وترتفع درجة غليانها وانصهارها، وتزداد أيضاً قدرتها على الذوبان في الماء. كما تنخفض طاقة التأين الأولى (الطاقة اللازمة لنزع إلكترون) مع زيادة الحجم الذري.
3. أحادية الذرة (Monatomic)
على عكس معظم الغازات الأخرى (مثل الأكسجين O₂ أو النيتروجين N₂)، تتواجد الغازات النبيلة في صورة ذرات مفردة وليست جزيئات ثنائية الذرة. وهذا أيضاً نتيجة لاستقرارها الإلكتروني الذي لا يحتاج إلى الارتباط مع ذرات أخرى.
4. عدم التوصيل الكهربائي في الظروف العادية
لكن عند تطبيق فرق جهد كافٍ (في أنابيب تفريغ الغاز)، تتأين ذراتها وتصبح موصلة للكهرباء، وتنبعث منها ألوان مميزة لكل غاز. هذه الخاصية هي أساس استخداماتها في الإضاءة.
ما هي أهمية الغازات النبيلة في حياتنا اليومية؟
للغازات النبيلة أهمية كبرى، حيث تستخدم في مجالات متنوعة بفضل خمولها الكيميائي وخصائصها الضوئية الفريدة:
- الإضاءة الحديثة: النيون للأضواء المميزة، والأرجون في المصابيح الكهربائية، والزينون في مصابيح السيارات المتطورة.
- اللحام والصناعة: يستخدم الأرجون كغاز واقٍ (تدريع) في لحام المعادن النشطة كالألومنيوم والتيتانيوم لمنع تأكسدها.
- الطب: يستخدم الزينون كغاز مخدر نظراً لآثاره الفسيولوجية، ويستخدم الهيليوم في تبريد مغناطيسات أجهزة الرنين المغناطيسي.
- البحث العلمي والتقنيات المتقدمة: يستخدم الكريبتون والزينون في الليزرات، ويستخدم نظير الكريبتون-86 كمعيار لقياس الأطوال (تاريخياً).
- التطبيقات الفضائية والطيران: يستخدم الهيليوم لضغط خزانات الوقود في الصواريخ لكونه خاملاً وخفيفاً.
هل تبحث عن مواد كيمياء عالية النقاء ؟ يمكنك زيارة متجر عالم الكيماويات للمواد الخام والكيماويات، حيث نوفر مجموعة متنوعة من المواد الكيميائية والمواد الخام.
المصادر والمراجع
اعتمدت في هذا الدليل على مصادر علمية موثوقة لضمان الدقة والمصداقية:
- Encyclopaedia Britannica – “Noble gas” – تاريخ الاطلاع: أبريل 2026 – https://www.britannica.com/science/noble-gas
- Encyclopaedia Britannica – “Argon” – تاريخ الاطلاع: أبريل 2026 – https://www.britannica.com/science/argon-chemical-element
- Royal Society of Chemistry – “Krypton” – تاريخ الاطلاع: أبريل 2026 – https://www.rsc.org/periodic-table/element/36/krypton
- Vedantu – “What are Noble Gases” – تاريخ الاطلاع: أبريل 2026 – https://www.vedantu.com/chemistry/what-are-noble-gases
- ScienceDaily – “Noble gas” – تاريخ الاطلاع: أبريل 2026 – https://www.sciencedaily.com/terms/noble_gas.htm
أسئلة شائعة حول الغازات النبيلة
لماذا تسمى الغازات النبيلة بهذا الاسم؟
كانت تسمى سابقاً “الغازات الخاملة” (Inert Gases) بسبب اعتقاد أنها لا تتفاعل. تم تغيير الاسم إلى “الغازات النبيلة” (Noble Gases) تشبيهاً بالمعادن النبيلة كالذهب والبلاتين التي تقاوم التفاعل الكيميائي. هذا الاسم يعكس طبيعتها بشكل أدق.
هل يمكن للغازات النبيلة أن تشكل مركبات كيميائية؟
نعم، على عكس الاعتقاد السابق، أثبت الكيميائي نيل بارتليت عام 1962 أن الزينون يمكنه تكوين مركبات مثل سداسي فلورو بلاتينات الزينون. وبعدها تم تحضير مركبات للكريبتون والرادون أيضاً. أثقل الغازات النبيلة تكون أكثر قدرة على تكوين المركبات.
ما هي الطريقة المتبعة لاستخلاص الغازات النبيلة من الهواء؟
يتم فصل الغازات النبيلة عن الهواء باستخدام طريقة التقطير التجزيئي للهواء المسال. يُبرد الهواء حتى يصبح سائلاً، ثم يتم تسخينه تدريجياً. وبما أن كل غاز له درجة غليان مختلفة، فإنها تتبخر وتنفصل عند درجات حرارة محددة. يتبخر الأرجون أولاً ثم النيون ثم الهيليوم وهكذا.
هل غاز الرادون خطير على الصحة؟
نعم، الرادون غاز مشع ينتج من التحلل الطبيعي لليورانيوم في التربة. قد يتسرب إلى المنازل عبر الشقوق في الأساسات، ويتراكم في الأماكن المغلقة. استنشاق الرادون هو السبب الثاني لسرطان الرئة بعد التدخين، وفقاً لوكالة حماية البيئة الأمريكية (EPA). يُنصح بفحص المنازل في المناطق المعرضة للخطر.




💬 التعليقات