الفرق بين الأيون والإلكترون
- الفرق بين الأيون والإلكترون
- جدول مقارنة بين الأيون والإلكترون
- علاقة الإلكترون بتكوين الأيون
- الأسئلة الشائعة
- هل الأيون والإلكترون نفس الشيء؟
- كم عدد الإلكترونات في الأيون؟
- هل يمكن رؤية الإلكترون أو الأيون بالعين المجردة؟
- ما الفرق بين الإلكترون الحر والأيون السالب؟
- لماذا تتحرك الإلكترونات بينما الأيونات تتحرك أبطأ؟
- المصادر والمراجع
هل تعتقد أن الأيون والإلكترون هما نفس الشيء؟ كثير من الناس يخلطون بينهما. لكن الحقيقة أن الإلكترون هو جزء من الذرة، بينما الأيون هو ذرة كاملة لكنها فقدت أو اكتسبت إلكترونات. في هذا المقال، سنوضح الفرق بين الأيون والإلكترون بشكل بسيط وواضح، وستفهم لماذا لا يمكن مقارنتهما كشيء واحد.
الفرق بين الأيون والإلكترون
الفرق الجوهري هو أن الإلكترون جسيم أولي، بينما الأيون هو ذرة متكاملة (لها نواة وإلكترونات) لكن بعدد إلكترونات غير متساوٍ. الإلكترون أصغر بآلاف المرات من الأيون. أيضاً، الأيون يمكن أن يكون موجباً أو سالباً، بينما الإلكترون دائماً سالب الشحنة.
موقع DifferenceBetween يذكر أن الإلكترونات هي التي تحدد شحنة الأيون؛ فزيادتها أو نقصانها هي ما يخلق الأيون.
جدول مقارنة بين الأيون والإلكترون
| وجه المقارنة | الإلكترون (Electron) | الأيون (Ion) |
|---|---|---|
| التعريف | جسيم دون ذري سالب الشحنة | ذرة أو جزيء فقد أو اكتسب إلكترونات |
| الحجم النسبي | صغير جداً (لا يكاد يُذكر مقارنة بالذرة) | كبير (حجم الذرة نفسها) |
| الشحنة | سالبة دائماً (-1) | موجبة (كاتيون) أو سالبة (أنيون) |
| المكونات | جسيم أولي لا يتكون من شيء أصغر | نواة (بروتونات + نيوترونات) + إلكترونات |
| الموقع | يدور حول النواة في الذرة، أو حر في المواد الموصلة | في المحاليل، البلورات الأيونية، أو كغاز |
| الاستقرار | مستقر في الذرة، لكن يمكن أن يتحرك بسهولة | مستقر نسبياً (الأيونات المنفردة نشطة لكنها موجودة) |
علاقة الإلكترون بتكوين الأيون
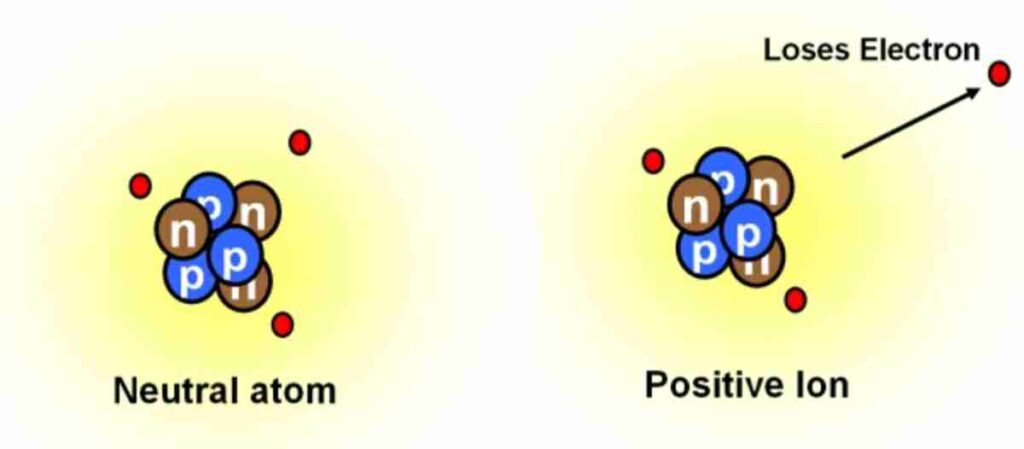
هنا يكمن السر: الأيونات تتكون بفضل الإلكترونات. عندما تفقد الذرة إلكتروناً واحداً أو أكثر، يصبح عدد البروتونات أكبر من عدد الإلكترونات، فتصبح الذرة أيوناً موجباً. وعندما تكتسب الذرة إلكترونات، يصبح عدد الإلكترونات أكبر من البروتونات، فتصبح أيوناً سالباً. إذاً، الإلكترونات هي “المنظم” لشحنة الأيون. بدون حركة الإلكترونات، لن تتكون أيونات.
مثال توضيحي: ذرة الصوديوم المتعادلة (11 بروتون، 11 إلكترون) تفقد إلكتروناً واحداً، فتصبح أيون الصوديوم الموجب (Na⁺) (11 بروتون، 10 إلكترونات). ذرة الكلور المتعادلة (17 بروتون، 17 إلكترون) تكتسب إلكتروناً، فتصبح أيون الكلوريد السالب (Cl⁻) (17 بروتون، 18 إلكترون).
هذه العلاقة هي أساس الكيمياء الكهربائية. لفهم كيف تتحرك الإلكترونات لتكوين الأيونات في البطاريات، يمكنك قراءة مقالنا عن ما هي الكيمياء الكهربائية؟
أيضاً، في تفاعلات الأكسدة والاختزال، نرى أن الأكسدة هي فقدان إلكترونات (تكون أيونات موجبة) والاختزال هو اكتساب إلكترونات (تكون أيونات سالبة). هذا يؤكد العلاقة الوثيقة بين الإلكترونات والأيونات.
الخلاصة: الإلكترون هو الجسيم الذي يتحرك، والأيون هو نتيجة حركته. لا يمكن فصلهما في التفكير الكيميائي.
الأسئلة الشائعة
هل الأيون والإلكترون نفس الشيء؟
لا، الأيون هو ذرة مشحونة، بينما الإلكترون هو جسيم دون ذري. الإلكترون أصغر بآلاف المرات من الأيون.
كم عدد الإلكترونات في الأيون؟
يعتمد على نوع الأيون. أيون الصوديوم الموجب (Na⁺) له 10 إلكترونات (فقد واحد). أيون الكلوريد السالب (Cl⁻) له 18 إلكتروناً (اكتسب واحداً). الأيون المتعادل ليس أيوناً أصلاً.
هل يمكن رؤية الإلكترون أو الأيون بالعين المجردة؟
لا، لا يمكن رؤية الإلكترونات أو الأيونات الفردية بالعين المجردة. يمكن رؤية تأثيراتها (مثل شرارات الكهرباء للإلكترونات، أو بلورات الملح للأيونات).
ما الفرق بين الإلكترون الحر والأيون السالب؟
الإلكترون الحر هو جسيم سالب منفرد. الأيون السالب (مثل Cl⁻) هو ذرة كاملة (نواة وإلكترونات) لكن لديها إلكترون زائد. الإلكترون الحر أصغر بكثير وأكثر نشاطاً.
لماذا تتحرك الإلكترونات بينما الأيونات تتحرك أبطأ؟
لأن كتلة الإلكترون صغيرة جداً، فيتحرك بسرعة كبيرة. الأيون ثقيل (له نواة) فيتحرك أبطأ في المحاليل أو في الموصلات.




💬 التعليقات