ما هي الكيمياء الكهربائية
- ما هي الكيمياء الكهربائية؟
- كيفية إنتاج الكيمياء الكهربائية (طرق إنتاجها)
- أولاً: إنتاج تيار كهربائي من تفاعل كيميائي تلقائي (الخلايا الجلفانية)
- ثانياً: إحداث تفاعل كيميائي باستخدام تيار كهربائي (الخلايا الإلكتروليتية)
- ما هي الخلية الكهروكيميائية؟
- أنواع الخلية الكهروكيميائية
- أولاً: الخلية الجلفانية (Galvanic Cell أو Voltaic Cell)
- ثانياً: الخلية الإلكتروليتية (Electrolytic Cell)
- جدول مقارنة: الخلية الجلفانية مقابل الخلية الإلكتروليتية
- خلاصة وتطبيقات يومية
- الأسئلة الشائعة
- ما الفرق بين الخلية الجلفانية والإلكتروليتية من حيث اتجاه تدفق الإلكترونات؟
- هل يمكن استخدام الخلية الجلفانية كخلية إلكتروليتية؟
- ما هو الإلكتروليت؟ أعطني أمثلة.
- لماذا تستخدم القنطرة الملحية في الخلايا الجلفانية؟
- هل التفاعل في الخلية الإلكتروليتية تلقائي؟
- المصادر والمراجع
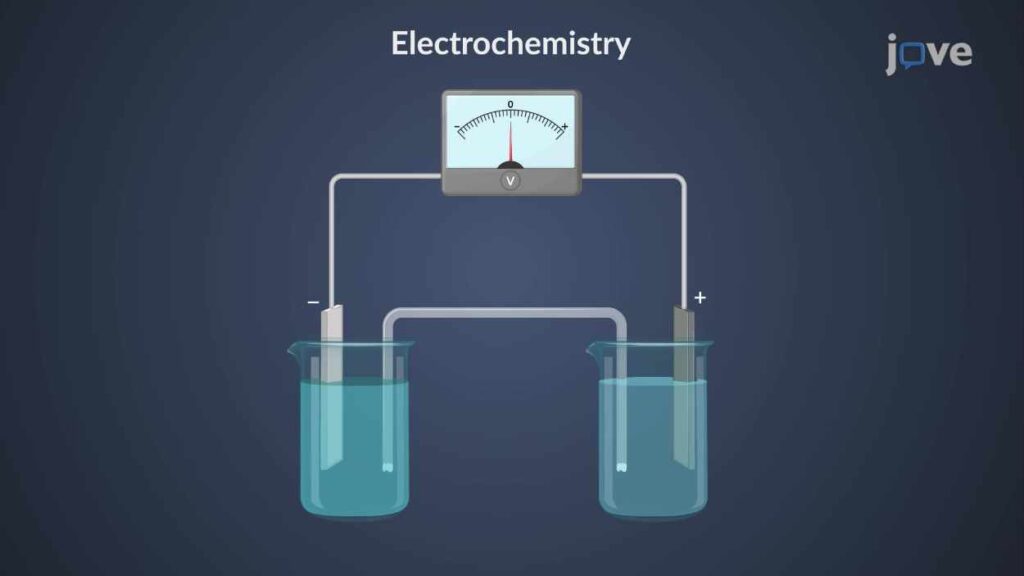
ما هي الكيمياء الكهربائية؟
الكيمياء الكهربائية (Electrochemistry) هي فرع من الكيمياء يدرس العلاقة بين الكهرباء والتفاعلات الكيميائية. ببساطة، هي علم تحويل الطاقة الكيميائية إلى طاقة كهربائية (كما في البطاريات)، وتحويل الطاقة الكهربائية إلى طاقة كيميائية (كما في عملية الطلاء الكهربائي أو تحليل الماء). قلب هذا العلم هو حركة الإلكترونات من مادة إلى أخرى خلال تفاعلات الأكسدة والاختزال.
تخيل أن مادتين مختلفتين (مثل الزنك والنحاس) توضعان في محلول مناسب. إحداهما تميل إلى فقدان إلكترونات (تتأكسد)، والأخرى تميل إلى اكتساب إلكترونات (تختزل). إذا وصّلتهما بسلك خارجي، تنتقل الإلكترونات عبر السلك مولدة تياراً كهربائياً. هذا هو أساس البطارية.
يذكر موقع Britannica أن الكيمياء الكهربائية تشمل دراسة الخلايا الجلفانية (التي تنتج تياراً) والخلايا الإلكتروليتية (التي يمر فيها تيار لإحداث تفاعل).
كيفية إنتاج الكيمياء الكهربائية (طرق إنتاجها)
الكيمياء الكهربائية ليست “شيئاً” ننتجه، بل هي عملية تحدث بطرق مختلفة. هناك طريقتان رئيسيتان:
أولاً: إنتاج تيار كهربائي من تفاعل كيميائي تلقائي (الخلايا الجلفانية)
هذه هي الطريقة التي تعمل بها البطاريات. عندما نضع معدنين مختلفين في إلكتروليت (محلول يوصل الكهرباء)، يحدث تفاعل أكسدة-اختزال تلقائي يولد تياراً كهربائياً في سلك خارجي. الطاقة الكهربائية المنتجة تأتي من الطاقة الكيميائية المخزنة في المواد المتفاعلة. مثال: بطارية السيارة الرصاصية الحمضية.
ثانياً: إحداث تفاعل كيميائي باستخدام تيار كهربائي (الخلايا الإلكتروليتية)
هنا العكس: نمرر تياراً كهربائياً من مصدر خارجي (بطارية خارجية) عبر محلول أو مصهور أيوني، مما يجبر تفاعلات الأكسدة والاختزال على الحدوث في الاتجاه غير التلقائي. هذا يستخدم في صناعة الكلور وهيدروكسيد الصوديوم، وفي طلاء المعادن، وفي تنقية النحاس.
موقع Byjus يشرح هذين النوعين من العمليات مع أمثلة توضيحية.
ما هي الخلية الكهروكيميائية؟
الخلية الكهروكيميائية (Electrochemical Cell) هي الجهاز الأساسي الذي يحدث فيه التحويل بين الطاقة الكيميائية والكهربائية. تتكون الخلية من مكونين رئيسيين:
- قطبان كهربائيان (Electrodes): وهما موصلان كهربائيان (معدنان عادةً). أحدهما يسمى “الأنود” (Anode) حيث تحدث الأكسدة (فقدان إلكترونات)، والآخر يسمى “الكاثود” (Cathode) حيث يحدث الاختزال (اكتساب إلكترونات).
- إلكتروليت (Electrolyte): محلول أو مصهور يحتوي على أيونات حرة تتحرك وتنقل التيار الكهربائي داخل الخلية.
- قنطرة ملحية (Salt Bridge) أو غشاء مسامي: يسمح بمرور الأيونات بين نصفي الخلية للحفاظ على التعادل الكهربائي.
تتصل الأقطاب بسلك خارجي يمر من خلاله الإلكترونات، ويمكن توصيل جهاز (مثل فولتميتر أو لمبة) لقياس أو استخدام التيار المنتج.
أنواع الخلية الكهروكيميائية
هناك نوعان رئيسيان من الخلايا الكهروكيميائية، يختلفان في وظيفتهما واتجاه التفاعل:
أولاً: الخلية الجلفانية (Galvanic Cell أو Voltaic Cell)
هي الخلية التي تحول الطاقة الكيميائية إلى طاقة كهربائية بشكل تلقائي. التفاعل الكيميائي داخلها يحدث من تلقاء نفسه، ويولد تياراً كهربائياً يمكن استخدامه لتشغيل جهاز. جميع البطاريات (الجافة، القلوية، الرصاصية) هي خلايا جلفانية. مثال بسيط: خلية دانيال (Daniel cell) التي تستخدم قطب زنك في محلول كبريتات الزنك، وقطب نحاس في محلول كبريتات النحاس، وتولد فرق جهد حوالي 1.1 فولت.
ثانياً: الخلية الإلكتروليتية (Electrolytic Cell)
هي الخلية التي تحول الطاقة الكهربائية إلى طاقة كيميائية. تحتاج إلى مصدر خارجي للتيار (بطارية خارجية أو مقوم تيار) لإجبار التفاعل الكيميائي على الحدوث. تستخدم هذه الخلايا في العمليات الصناعية مثل:
- التحليل الكهربائي للماء: لإنتاج غازي الهيدروجين والأكسجين.
- طلاء المعادن (Electroplating): طلاء الفضة أو الذهب أو الكروم على المعادن الرخيصة.
- تنقية النحاس.
- إنتاج الصوديوم والكلور من مصهور كلوريد الصوديوم.
موقع LibreTexts يقدم شرحاً متكاملاً عن أنواع الخلايا الكهروكيميائية.
جدول مقارنة: الخلية الجلفانية مقابل الخلية الإلكتروليتية
| وجه المقارنة | الخلية الجلفانية | الخلية الإلكتروليتية |
|---|---|---|
| تحويل الطاقة | كيميائية → كهربائية | كهربائية → كيميائية |
| التفاعل | تلقائي (يحدث من نفسه) | غير تلقائي (يحتاج طاقة كهربائية) |
| شحنة الأنود والكاثود | الأنود سالب (تفقد إلكترونات)، الكاثود موجب | الأنود موجب (مرتبط بالقطب الموجب للمصدر)، الكاثود سالب |
| أمثلة | بطاريات السيارات، البطاريات الجافة، الخلايا القلوية | طلاء المعادن، تحليل الماء، تنقية النحاس |
قد تخلط بين الأنود والكاثود في البداية، لكن تذكر قاعدة بسيطة: “الأنود هو مكان الأكسدة (فقدان إلكترونات)” بغض النظر عن نوع الخلية. في الخلية الجلفانية، الأنود سالب لأن الإلكترونات تنطلق منه. في الخلية الإلكتروليتية، الأنود موجب لأنه يسحب الإلكترونات من المحلول.
إذا كنت مهتماً بتطبيقات المواد الكيميائية في الصناعة، يمكنك قراءة مقالنا عن ما هي السيليكونات؟.
خلاصة وتطبيقات يومية
الكيمياء الكهربائية ليست مجرد موضوع أكاديمي، بل هي جزء من حياتك اليومية. كل مرة تستخدم فيها هاتفك، أو تشغل سيارتك، أو تشاهد التلفاز، فأنت تستخدم مبادئ الكيمياء الكهربائية. حتى عملية توصيل الإشارات العصبية في جسمك تعتمد على حركة الأيونات (وهي كيمياء كهربائية حيوية).
تذكر: الكيمياء الكهربائية هي علم تحويل الطاقة بين الصورتين الكيميائية والكهربائية. وتتم عبر خليتين رئيسيتين: الجلفانية (تنتج تياراً) والإلكتروليتية (تستخدم تياراً).
الأسئلة الشائعة
ما الفرق بين الخلية الجلفانية والإلكتروليتية من حيث اتجاه تدفق الإلكترونات؟
في الخلية الجلفانية، تتدفق الإلكترونات تلقائياً من الأنود (القطب السالب) إلى الكاثود (الموجب) عبر السلك الخارجي. في الخلية الإلكتروليتية، يفرض المصدر الخارجي اتجاه الإلكترونات عكسياً، فتتدفق من القطب السالب للمصدر إلى الكاثود (القطب السالب للخلية).
هل يمكن استخدام الخلية الجلفانية كخلية إلكتروليتية؟
نعم، بعض الخلايا قابلة للعكس. بطارية السيارة (الرصاصية الحمضية) تعمل كخلية جلفانية عندما تفرغ (تنتج تياراً)، وتعمل كخلية إلكتروليتية عندما تشحن (يمر تيار لإعادة شحنها).
ما هو الإلكتروليت؟ أعطني أمثلة.
الإلكتروليت هو مادة تحتوي على أيونات حرة تسمح بمرور التيار الكهربائي. أمثلة: المحاليل الملحية مثل الماء المالح، الأحماض مثل حمض الكبريتيك، القواعد مثل هيدروكسيد الصوديوم المذاب، أو الأملاح المنصهرة مثل كلوريد الصوديوم المصهور.
لماذا تستخدم القنطرة الملحية في الخلايا الجلفانية؟
للحفاظ على التعادل الكهربائي في المحلولين. بدونها، سيتراكم الشحنات الموجبة في نصف الخلية الذي يحدث فيه الأكسدة (لأن أيونات الزنك الموجبة تنتقل إلى المحلول)، والشحنات السالبة في نصف الخلية الآخر، وسيتوقف التفاعل بسرعة.
هل التفاعل في الخلية الإلكتروليتية تلقائي؟
لا، التفاعل في الخلية الإلكتروليتية غير تلقائي. يحتاج إلى مصدر خارجي للتيار الكهربائي لدفع التفاعل في الاتجاه المعاكس لاتجاهه التلقائي. هذه هي الطريقة التي نستخدمها لشحن البطاريات أو طلاء المعادن.




💬 التعليقات