تحليل الماء كهربائياً : التفاعل والاستخدامات
- ما هو تحليل الماء كهربائياً؟
- كيف تتم طريقة تحليل الماء كهربائياً خطوة بخطوة؟
- ما هي معادلة التحليل الكهربائي للماء؟
- ما هي استخدامات التحليل الكهربائي؟
- المصادر والمراجع
- أسئلة شائعة حول تحليل الماء كهربائياً
- لماذا لا يتحلل الماء النقي كهربائياً بسهولة؟
- ما هو مصدر الطاقة المثالي لتحليل الماء كهربائياً؟
- هل يمكن إنتاج الهيدروجين من تحليل الماء بكفاءة عالية؟
- ما الفرق بين التحليل الكهربائي القلوي وتحليل PEM؟
هل يمكننا تحويل كوب من الماء إلى وقود؟ الإجابة هي نعم، من خلال عملية رائعة تسمى تحليل الماء كهربائياً (التحليل الكهربائي للماء). هذه التقنية، التي تستخدم التيار الكهربائي لتقسيم جزيء الماء (H₂O) إلى عناصره الأساسية: الهيدروجين (H₂) والأكسجين (O₂)، تحمل مفتاحاً لمستقبل الطاقة النظيفة. في هذا الدليل، سنتعرف على مفهوم هذه العملية، وآليتها، والمعادلة الكيميائية لها، واستخداماتها المتعددة.
ما هو تحليل الماء كهربائياً؟
تحليل الماء كهربائياً (Electrolysis of Water) هو عملية كيميائية تستخدم تياراً كهربائياً لتكسير جزيء الماء إلى غازي الهيدروجين والأكسجين. تحدث هذه العملية في جهاز يسمى “المحلل الكهربائي”، حيث يمر التيار عبر الماء (مع إضافة إلكتروليت مثل حمض الكبريتيك لزيادة التوصيلية) مما يؤدي إلى أكسدة واختزال جزيئات الماء على سطح الأقطاب الكهربائية (الأنود والكاثود). ينتج عن ذلك غاز الأكسجين عند القطب الموجب (الأنود) وغاز الهيدروجين عند القطب السالب (الكاثود).
كيف تتم طريقة تحليل الماء كهربائياً خطوة بخطوة؟
لتنفيذ تحليل الماء كهربائياً بنفسك (على نطاق صغير)، يمكنك اتباع هذه الخطوات البسيطة:
- تحضير المحلول: املأ كأساً زجاجياً بالماء وأضف إليه كمية قليلة من الإلكتروليت مثل كبريتات الصوديوم (Na₂SO₄) أو حمض الكبريتيك (H₂SO₄) لزيادة قدرة الماء على توصيل الكهرباء.
- وضع الأقطاب: اغمر قطبين كهربائيين خاملين (عادةً من البلاتين أو الجرافيت) في المحلول. هذه الأقطاب لا تتفاعل مع الماء ويُطلق على القطب الموجب اسم “الأنود” والقطب السالب اسم “الكاثود”.
- توصيل التيار الكهربائي: قم بتوصيل الأقطاب بمصدر تيار مستمر (DC) مثل بطارية. ستلاحظ تكون فقاعات من الغاز حول القطبين فوراً.
- جمع الغازات: يمكنك وضع أنابيب اختبار مقلوبة فوق كل قطب لجمع الغازات المتصاعدة. الأنبوب فوق الكاثود (القطب السالب) يجمع غاز الهيدروجين، والأنبوب فوق الأنود (القطب الموجب) يجمع غاز الأكسجين.
ستلاحظ أن كمية غاز الهيدروجين المتولدة هي ضعف كمية غاز الأكسجين، وهذا يتوافق مع الصيغة الجزيئية للماء (H₂O).
ما هي معادلة التحليل الكهربائي للماء؟
تتضمن عملية تحليل الماء كهربائياً تفاعلين نصفين:
- عند الكاثود (القطب السالب – الاختزال): 2H₂O(l) + 2e⁻ → H₂(g) + 2OH⁻(aq)
- عند الأنود (القطب الموجب – الأكسدة): 2H₂O(l) → O₂(g) + 4H⁺(aq) + 4e⁻
والمعادلة الكلية للتفاعل هي: 2H₂O(l) → 2H₂(g) + O₂(g)
هذه المعادلة تبين أنه من جزيئين من الماء، نحصل على جزيئين من غاز الهيدروجين وجزيء واحد من غاز الأكسجين.
ما هي استخدامات التحليل الكهربائي؟
للتحليل الكهربائي تطبيقات واسعة ومهمة تتجاوز مجرد تجربة مختبرية:
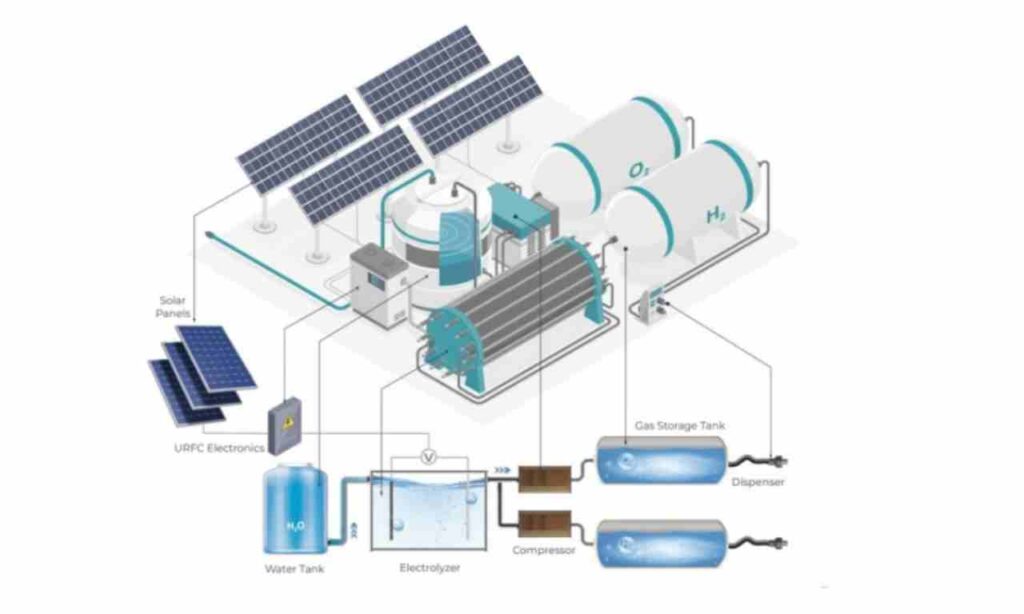
- إنتاج الهيدروجين الأخضر: يعتبر تحليل الماء كهربائياً باستخدام كهرباء من مصادر متجددة (طاقة شمسية أو رياح) من أنظف الطرق لإنتاج الهيدروجين، الذي يُستخدم كوقود نظيف للسيارات وفي الصناعة.
- الطلاء الكهربائي (Electroplating): يستخدم لطلاء المعادن (مثل طلاء الفضة أو الذهب على النحاس) لحمايتها من التآكل أو تحسين مظهرها.
- تنقية المعادن: يستخدم في تنقية معادن مثل النحاس والألمنيوم من شوائبها.
- صناعة المواد الكيميائية: يستخدم لإنتاج الكلور وهيدروكسيد الصوديوم من محلول ملحي (التحليل الكهربائي للمحلول الملحي).
- إنتاج الأكسجين في الغواصات والمركبات الفضائية: تستخدم أنظمة التحليل الكهربائي لتوفير الأكسجين القابل للتنفس في الأماكن المغلقة.
كما أنصحك بالاطلاع على تطبيقات الخلايا الكهروكيميائية لمعرفة المزيد.
المصادر والمراجع
اعتمدت في هذا الدليل على مصادر علمية موثوقة:
- Chemistry LibreTexts – “23.9: Electrolysis of Water” – شرح تفصيلي للعملية والمعادلات – تاريخ الاطلاع: أبريل 2026 – https://chem.libretexts.org/…/23.09%3A_Electrolysis_of_Water
- U.S. Department of Energy – “Hydrogen Production: Electrolysis” – تاريخ الاطلاع: أبريل 2026 – https://www.energy.gov/eere/fuelcells/hydrogen-production-electrolysis
- ScienceDirect – “Water Electrolysis” – نظرة عامة أكاديمية – تاريخ الاطلاع: أبريل 2026 – https://www.sciencedirect.com/topics/engineering/water-electrolysis
- BYJU’S – “Water Electrolysis” – شرح مبسط مع الرسوم – تاريخ الاطلاع: أبريل 2026 – https://byjus.com/jee/water-electrolysis/
أسئلة شائعة حول تحليل الماء كهربائياً
لماذا لا يتحلل الماء النقي كهربائياً بسهولة؟
لأن الماء النقي موصلية كهربائية ضعيفة جداً بسبب نقص الأيونات. لذلك نضيف إلكتروليتاً (مثل حمض الكبريتيك أو كبريتات الصوديوم) لزيادة عدد الأيونات في المحلول، مما يحسن التوصيلية ويسمح بمرور التيار الكهربائي.
ما هو مصدر الطاقة المثالي لتحليل الماء كهربائياً؟
المصدر المثالي هو الكهرباء المتجددة (الطاقة الشمسية أو طاقة الرياح)، لأنها تنتج “الهيدروجين الأخضر” بدون انبعاثات كربونية. يمكن أيضاً استخدام الطاقة النووية أو الشبكة الكهربائية، لكنها قد تترك بصمة كربونية أعلى.
هل يمكن إنتاج الهيدروجين من تحليل الماء بكفاءة عالية؟
نعم، تصل كفاءة المحلل الكهربائي الحديث (خاصة نوع PEM) إلى 70-80%، مما يعني تحويل معظم الطاقة الكهربائية إلى طاقة كيميائية في الهيدروجين. الكفاءة تتطور باستمرار مع التقدم التكنولوجي.
ما الفرق بين التحليل الكهربائي القلوي وتحليل PEM؟
التحليل القلوي (Alkaline) أقدم وأرخص، ويستخدم إلكتروليتاً سائلاً (هيدروكسيد البوتاسيوم). تحليل PEM (غشاء تبادل البروتونات) أحدث، وأكثر كفاءة، ويشغل مساحة أصغر، لكنه أغلى ثمناً. كلا النوعين يستخدمان لإنتاج الهيدروجين.




💬 التعليقات