حالات المادة الثلاث
- ما هي حالات المادة ؟
- ما هي خصائص الحالة الصلبة؟
- ما هي خصائص الحالة السائلة؟
- ما هي خصائص الحالة الغازية؟
- كيف تتحول المادة من حالة إلى أخرى؟
- ما هي عملية الانصهار (Melting)؟
- ما هي عملية التجمد (Freezing)؟
- ما هي عملية التبخر (Evaporation)؟
- ما هي عملية التكاثف (Condensation)؟
- ما هي عملية التسامي (Sublimation)؟
- المصادر والمراجع
- الأسئلة الشائعة
- ما هي حالة البلازما؟
- كيف تؤثر الحرارة على حركة الجزيئات في حالات المادة؟
- هل يمكن للمادة أن تكون في حالة صلبة وسائلة في نفس الوقت؟
- ما الفرق بين التبخر والغليان؟
هل تساءلت يوماً لماذا يحافظ الكتاب على شكله بينما يأخذ الماء شكل الإناء الذي يوضع فيه؟ ولماذا ينتشر العطر في كل أرجاء الغرفة؟ الإجابة تكمن في حالات المادة. في هذا الدليل، سنستعرض حالات المادة الثلاث الأساسية: الصلبة، والسائلة، والغازية، ونكتشف كيف تتحول المادة من حالة إلى أخرى في حياتنا اليومية.
ما هي حالات المادة ؟
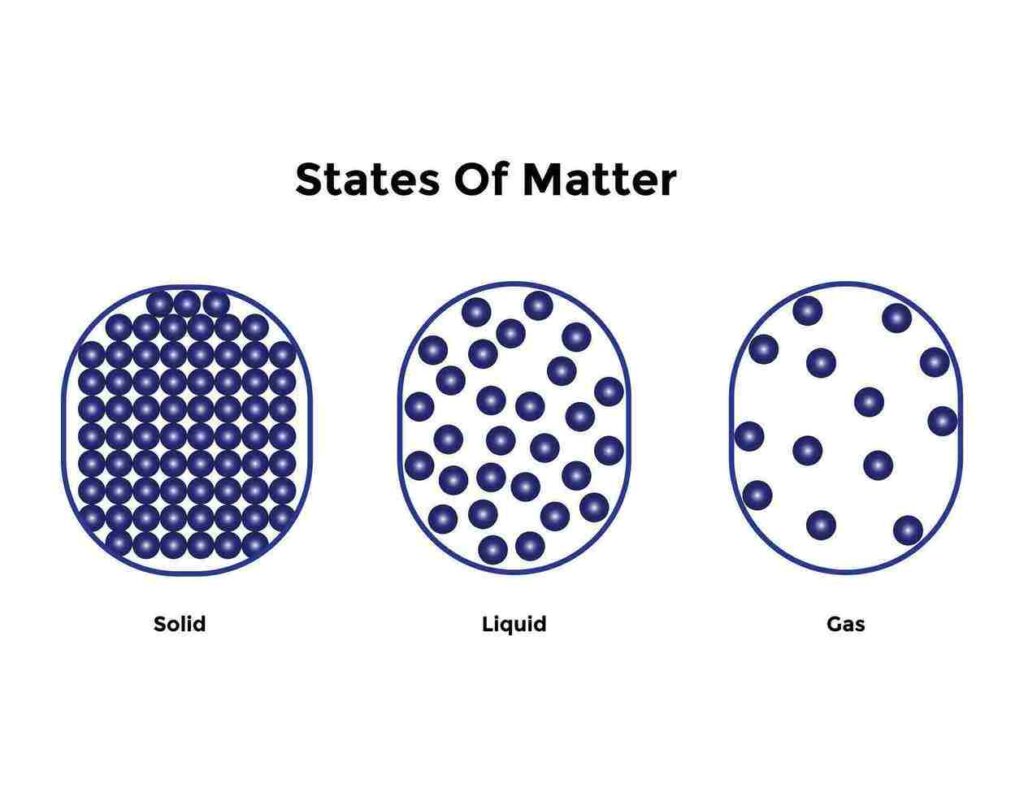
حالات المادة هي الأشكال المختلفة التي توجد عليها المادة، وتتحدد بناءً على ترتيب جزيئاتها ودرجة تماسكها وطاقتها الحركية. المادة من حولنا (الماء، الهواء، الصخر) توجد في إحدى ثلاث حالات رئيسية: الصلبة، والسائلة، والغازية.
ما هي خصائص الحالة الصلبة؟
في الحالة الصلبة، تكون الجزيئات متقاربة جداً ومترابطة بقوى تجاذب قوية، ولا تستطيع التحرك بحرية، بل تهتز في أماكنها فقط.
- شكل ثابت وحجم ثابت: للمادة الصلبة شكلها الخاص الذي لا يتغير إلا بقوة خارجية.
- كثافة عالية: الجزيئات قريبة من بعضها، مما يجعل المواد الصلبة غالباً ذات كثافة عالية.
- لا تنتشر: جزيئات المادة الصلبة لا تنتشر في الوعاء لأنها محصورة في مكانها.
أمثلة على المواد الصلبة: الحديد، الخشب، الجليد، الصخر.
ما هي خصائص الحالة السائلة؟
في الحالة السائلة، تكون الجزيئات أقل ترابطاً من الصلبة، وتستطيع الانزلاق والتدفق فوق بعضها البعض، لكنها تبقى متقاربة نسبياً.
- حجم ثابت وشكل متغير: يأخذ السائل شكل الإناء الذي يوضع فيه، لكن حجمه يبقى ثابتاً.
- كثافة متوسطة: أقل كثافة من المواد الصلبة عادة، وأعلى من الغازات.
- قابلية للجريان والانتشار: تتدفق الجزيئات وتتحرك بسهولة، لكنها تنتشر ببطء نسبياً.
أمثلة على المواد السائلة: الماء، الزيت، الحليب، الزئبق.
ما هي خصائص الحالة الغازية؟
في الحالة الغازية، تكون الجزيئات متباعدة جداً، وتتحرك بسرعة عشوائية كبيرة، وتتصادم مع بعضها البعض ومع جدران الوعاء.
- شكل وحجم متغيران: ينتشر الغاز ليملأ أي وعاء يوضع فيه، متخذاً شكله وحجمه.
- كثافة منخفضة: الجزيئات متباعدة، لذا كثافة الغازات منخفضة جداً.
- سهولة الانضغاط والانتشار: يمكن ضغط الغاز بسهولة، وينتشر بسرعة كبيرة في الفراغ المتاح.
أمثلة على المواد الغازية: الهواء، بخار الماء، الأكسجين، غاز الميثان.
كيف تتحول المادة من حالة إلى أخرى؟
يمكن للمادة أن تتحول من حالة من حالات المادة إلى أخرى عن طريق إضافة أو سحب الطاقة (الحرارة). هذه العملية فيزيائية وليست كيميائية، لأن تركيب المادة لا يتغير.
ما هي عملية الانصهار (Melting)؟
تحول المادة من الحالة الصلبة إلى السائلة عند امتصاصها للحرارة. مثال: ذوبان مكعب الثلج عند تركه خارج الفريزر.
ما هي عملية التجمد (Freezing)؟
تحول المادة من الحالة السائلة إلى الصلبة عند فقدانها للحرارة. مثال: تجمد الماء في قوالب الثلج داخل الفريزر.
ما هي عملية التبخر (Evaporation)؟
تحول المادة من الحالة السائلة إلى الغازية عند امتصاصها للحرارة. مثال: تبخر الماء من البرك والبحيرات بفعل حرارة الشمس.
ما هي عملية التكاثف (Condensation)؟
تحول المادة من الحالة الغازية إلى السائلة عند فقدانها للحرارة. مثال: تكاثف بخار الماء على سطح كوب بارد مملوء بمشروب مثلج.
ما هي عملية التسامي (Sublimation)؟
تحول المادة مباشرة من الحالة الصلبة إلى الغازية دون المرور بالحالة السائلة. مثال: تحول الثلج الجاف (CO₂ الصلب) إلى غاز مباشرة.
المصادر والمراجع
اعتمدت في هذا الشرح على مصادر علمية موثوقة:
- Live Science – “States of Matter: Facts” – تاريخ الاطلاع: أبريل 2026 – https://www.livescience.com/46506-states-of-matter.html
- Visionlearning – “States of Matter” – تاريخ الاطلاع: أبريل 2026 – https://www.visionlearning.com/en/library/Chemistry/1/States-of-Matter/120
- BYJU’S – “Difference Between Solid Liquid and Gas” – تاريخ الاطلاع: أبريل 2026 – https://byjus.com/chemistry/difference-between-solid-liquid-and-gas/
الأسئلة الشائعة
ما هي حالة البلازما؟
البلازما هي الحالة الرابعة للمادة، وتتكون من غاز متأين (جزيئاته فقدت أو اكتسبت إلكترونات). توجد في النجوم (بما فيها الشمس)، والبرق، ومصابيح الفلورسنت. لم نذكرها هنا لأنها أقل شيوعاً في حياتنا اليومية.
كيف تؤثر الحرارة على حركة الجزيئات في حالات المادة؟
كلما زادت الحرارة، زادت الطاقة الحركية للجزيئات. في المواد الصلبة، تهتز الجزيئات. في السائلة، تتحرك وتتدفق. في الغازية، تتحرك بسرعة عشوائية كبيرة. إضافة الحرارة كافية يمكن أن تغير حالة المادة.
هل يمكن للمادة أن تكون في حالة صلبة وسائلة في نفس الوقت؟
نعم، عند نقطة الانصهار، يمكن أن يتواجد الثلج (صلب) والماء (سائل) معاً في حالة توازن. هذا ما نراه عند ذوبان الثلج، حيث تختلط قطع الثلج مع الماء السائل.
ما الفرق بين التبخر والغليان؟
التبخر عملية سطحية تحدث عند أي درجة حرارة، وتتحول فيها جزيئات سطح السائل فقط إلى بخار. أما الغليان، فهو عملية تحدث عند درجة حرارة محددة (نقطة الغليان) وتشمل كل كتلة السائل، ويتكون بخار في داخل السائل (فقاعات).




💬 التعليقات