عدد النيوترونات في نواة الذرة
- كيف نحسب عدد النيوترونات؟
- مثال 1: حساب عدد نيوترونات ذرة الصوديوم
- مثال 2: حساب عدد نيوترونات ذرة الكربون
- ما هي أهمية عدد النيوترونات؟
- 1. استقرار النواة الذرية
- 2. النيوترونات والنظائر
- 3. الخواص النووية والنشاط الإشعاعي
- المراجع
- أسئلة شائعة حول عدد النيوترونات
- هل يمكن أن يختلف عدد النيوترونات في ذرات نفس العنصر؟
- كيف يمكنني حساب عدد النيوترونات إذا كنت أعرف العدد الكتلي فقط؟
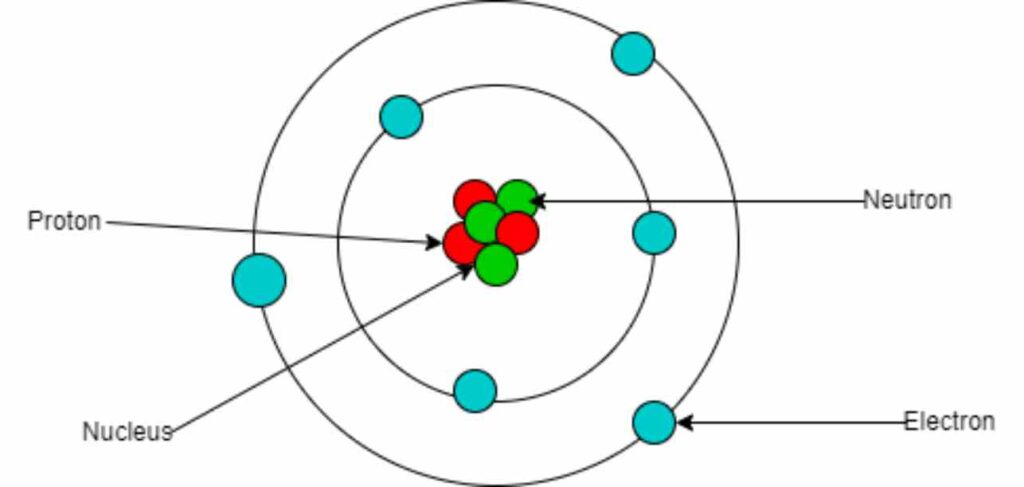
تُعتبر النيوترونات، إلى جانب البروتونات، اللبنات الأساسية لنواة الذرة. على عكس البروتونات التي تحمل شحنة موجبة، فإن النيوترونات متعادلة كهربائياً، وهذا يمنحها خصائص فريدة تؤثر في استقرار الذرة وكتلتها. في هذا الدليل، سنتعرف على طريقة حساب عدد النيوترونات في نواة الذرة، وأهمية هذا العدد في تحديد خصائص النواة.
كيف نحسب عدد النيوترونات؟
يمكن حساب عدد النيوترونات (N) ببساطة من خلال العلاقة: عدد النيوترونات = العدد الكتلي (A) – العدد الذري (Z).
أي أن: عدد النيوترونات = العدد الكتلي – عدد البروتونات.
مثال 1: حساب عدد نيوترونات ذرة الصوديوم
العدد الذري للصوديوم (Na) هو 11، والعدد الكتلي لأكثر نظائره شيوعاً (Na-23) هو 23. إذاً، عدد النيوترونات = 23 – 11 = 12 نيوتروناً.
مثال 2: حساب عدد نيوترونات ذرة الكربون
العدد الذري للكربون (C) هو 6. لنظير الكربون-12 (العدد الكتلي 12)، عدد النيوترونات = 12 – 6 = 6 نيوترونات. أما لنظير الكربون-14 (العدد الكتلي 14)، فعدد النيوترونات = 14 – 6 = 8 نيوترونات.
ملاحظة مهمة: كتلة الإلكترونات صغيرة جداً لدرجة أنه يمكن تجاهلها عند حساب عدد النيوترونات بهذه الطريقة.
ما هي أهمية عدد النيوترونات؟
لا يقتصر دور النيوترونات على مجرد إضافة كتلة للنواة، بل لها أهمية محورية في تحديد خصائص الذرة:
1. استقرار النواة الذرية
تعمل النيوترونات كـ “مادة لاصقة نووية” (Nuclear Glue). فهي تساعد في التغلب على قوى التنافر الكهربائي الشديدة بين البروتونات الموجبة، مما يحافظ على تماسك النواة. النسبة بين عدد النيوترونات وعدد البروتونات (n/p) تحدد استقرار النواة؛ فالنوى ذات النسبة المتوازنة تكون مستقرة، بينما تميل النوى غير المتوازنة إلى النشاط الإشعاعي (التحلل).
2. النيوترونات والنظائر
تلعب النيوترونات الدور الأساسي في تكوين النظائر؛ وهي ذرات لنفس العنصر تختلف فقط في عدد النيوترونات. للمزيد من التفاصيل حول هذا الموضوع، يمكنك مراجعة مقالنا المتخصص حول النظائر الكيميائية.
3. الخواص النووية والنشاط الإشعاعي
يُعد عدد النيوترونات عاملاً حاسماً في تحديد ما إذا كانت النواة مستقرة أم مشعة. النوى التي تحتوي على عدد كبير جداً أو قليل جداً من النيوترونات مقارنة بعدد البروتونات تكون غير مستقرة، وتسعى للوصول إلى حالة أكثر استقراراً عن طريق التحلل الإشعاعي، أي انبعاث جسيمات وطاقة
المراجع
اعتمدت في هذا الدليل على مصادر علمية موثوقة:
- الوكالة الدولية للطاقة الذرية (IAEA) – “ما النظائر؟” – تاريخ الاطلاع: أبريل 2026 – https://www.iaea.org/ar/newscenter/news/m-lnzyr
- عالم الكيماويات – “خصائص النيوترونات : الكتلة، الشحنة، ودورها في الذرة” – تاريخ الاطلاع: أبريل 2026 – https://chemicalsmed.com/خصائص-النيوترونات/
- WikiHow – “كيفية حساب عدد النيوترونات في الذرة” – تاريخ الاطلاع: أبريل 2026 – https://ar.wikihow.com/حساب-عدد-النيوترونات-في-الذرة
أسئلة شائعة حول عدد النيوترونات
هل يمكن أن يختلف عدد النيوترونات في ذرات نفس العنصر؟
نعم، هذه الذرات تُسمى “نظائر”. فجميع ذرات الكربون، على سبيل المثال، لها 6 بروتونات، ولكن يمكن أن تحتوي على 6 أو 7 أو 8 نيوترونات، لتشكل نظائر الكربون-12، والكربون-13، والكربون-14 على التوالي.
كيف يمكنني حساب عدد النيوترونات إذا كنت أعرف العدد الكتلي فقط؟
لا يمكن حساب عدد النيوترونات بدقة من العدد الكتلي وحده، لأن العدد الكتلي هو مجموع البروتونات والنيوترونات. يجب معرفة العدد الذري (عدد البروتونات) أولاً، ثم طرحه من العدد الكتلي.




💬 التعليقات