قانون الغازات المثالية
- قانون الغازات المثالية ؟
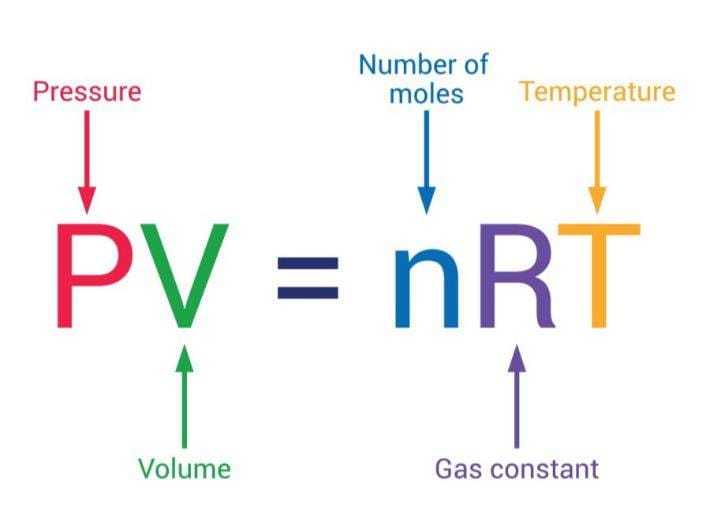
- معادلة الحالة: PV = nRT
- شرح متغيرات القانون
- فرضيات الغاز المثالي: متى يطبق القانون؟
- الغازات الحقيقية مقابل الغازات المثالية
- الخلاصة: القانون الذي يربط المتناقضات
- أسئلة شائعة حول قانون الغازات المثالية
- لماذا نستخدم الكلفن بدلاً من الدرجة المئوية؟
- متى يفشل قانون الغازات المثالية؟
- ما هو الفرق بين الثابت العام للغازات (R) وثابت بولتزمان؟
قانون الغازات المثالية ؟
يُعد قانون الغازات المثالية حجر الزاوية في الفيزياء والكيمياء الحرارية، حيث يوفر إطاراً رياضياً بسيطاً وقوياً لوصف سلوك الغازات تحت ظروف متنوعة. فـ قانون الغازات المثالية هو معادلة حالة تصف العلاقة بين الضغط، الحجم، درجة الحرارة، وكمية المادة للغاز الافتراضي الذي يتبع مجموعة من الفرضيات المبسطة. إن فهم قانون الغازات المثالية ليس مجرد تمرين أكاديمي، بل هو أداة حيوية يستخدمها المهندسون والعلماء لتصميم كل شيء، من محركات السيارات إلى أنظمة دعم الحياة في الفضاء، حيث تسعى المادة دائماً للتعبير عن طاقتها من خلال هذه المتغيرات الأربعة المتداخلة.
معادلة الحالة: PV = nRT
“تنص معادلة الغاز المثالي على أن حاصل ضرب ضغط الغاز في حجمه يساوي حاصل ضرب عدد مولاته في الثابت العام للغازات في درجة حرارته المطلقة.”
عند دراسة قانون الغازات المثالية، نستخدم الصيغة الرياضية الشهيرة PV = nRT، حيث يمثل كل رمز متغيراً فيزيائياً محدداً. للمزيد حول المواد والتركيبات الكيميائية، يمكنك زيارة موقع المواد الكيميائية المتخصص. من المهم ملاحظة أن درجة الحرارة يجب أن تُقاس دائماً بالكلفن (K) في هذه المعادلة لضمان دقة النتائج، حيث يبدأ مقياس كلفن من الصفر المطلق الذي تتوقف عنده حركة الجزيئات تماماً.
شرح متغيرات القانون
لفهم كيفية عمل قانون الغازات المثالية، يجب تفكيك عناصره الأساسية وفهم دور كل منها:
- الضغط (P): القوة التي تمارسها جزيئات الغاز على جدران الوعاء نتيجة التصادمات، ويُقاس عادة بالضغط الجوي (atm) أو الباسكال.
- الحجم (V): الحيز الذي يشغله الغاز، ويُقاس باللتر (L) أو المتر المكعب.
- عدد المولات (n): كمية المادة الموجودة في العينة الغازية.
- الثابت العام للغازات (R): قيمة ثابتة تربط بين الوحدات المستخدمة، وقيمتها الشائعة هي
0.0821 L.atm/mol.K. - درجة الحرارة (T): مقياس لمتوسط الطاقة الحركية للجزيئات، وتُحسب بجمع 273.15 مع الدرجة المئوية.
يمكنك الاطلاع على الاشتقاق التاريخي لهذا القانون عبر ويكيبيديا: قانون الغازات المثالية.
فرضيات الغاز المثالي: متى يطبق القانون؟
يعتمد قانون الغازات المثالية على نموذج مبسط للمادة يفترض الآتي:
- حجم الجزيئات مهمل: يُفترض أن جزيئات الغاز نقاط مادية ليس لها حجم مقارنة بحجم الوعاء الذي يحتويها.
- انعدام قوى التجاذب: يُفترض عدم وجود قوى تجاذب أو تنافر بين الجزيئات (قوى فان دير فالس).
- التصادمات المرنة: تُفترض أن التصادمات بين الجزيئات ومع جدران الوعاء مرنة تماماً، أي لا تضيع فيها الطاقة الحركية.
تؤكد برنامج الأمم المتحدة للبيئة (UNEP) على أهمية فهم سلوك الغازات في الغلاف الجوي، حيث يقترب الهواء الجوي من سلوك الغاز المثالي في الظروف العادية من الضغط والحرارة، مما يسهل نمذجة التغيرات المناخية.
الغازات الحقيقية مقابل الغازات المثالية
رغم قوة قانون الغازات المثالية، إلا أنه يظل نموذجاً تقريبياً. الغازات الحقيقية تحيد عن السلوك المثالي عند تعرضها لضغوط عالية جداً أو درجات حرارة منخفضة جداً. في هذه الظروف، يصبح حجم الجزيئات وقوى التجاذب بينها عوامل لا يمكن إهمالها، مما يتطلب استخدام معادلات أكثر تعقيداً مثل “معادلة فان دير فالس”. ومع ذلك، يظل القانون المثالي كافياً لمعظم التطبيقات الهندسية والعلمية اليومية.
الخلاصة: القانون الذي يربط المتناقضات
في الختام، يظل قانون الغازات المثالية واحداً من أجمل الأمثلة على كيفية تبسيط الطبيعة المعقدة في معادلة رياضية واحدة. من خلال ربط الضغط والحجم والحرارة، منحنا هذا القانون القدرة على التنبؤ بسلوك المادة الغازية وفهم العمليات الطبيعية والصناعية بدقة مذهلة. إن الغاز المثالي قد لا يوجد في الواقع بشكل مطلق، لكن قانونه يظل الحقيقة العلمية التي لا غنى عنها في رحلتنا لاستكشاف أسرار الكون المادي.
| المتغير | الرمز | الوحدة الشائعة | العلاقة مع الضغط (P) |
|---|---|---|---|
| الحجم | V | لتر (L) | عكسية (قانون بويل) |
| درجة الحرارة | T | كلفن (K) | طردية (قانون شارل) |
| عدد المولات | n | مول (mol) | طردية (قانون أفوجادرو) |
| الثابت العام | R | L.atm/mol.K | قيمة ثابتة للربط |
أسئلة شائعة حول قانون الغازات المثالية
لماذا نستخدم الكلفن بدلاً من الدرجة المئوية؟
نستخدم الكلفن في قانون الغازات المثالية لأن مقياس كلفن هو مقياس مطلق يبدأ من الصفر الحقيقي للطاقة، مما يمنع ظهور قيم سالبة للضغط أو الحجم في الحسابات الرياضية، وهو ما لا يتوافق مع الواقع الفيزيائي.
متى يفشل قانون الغازات المثالية؟
يفشل القانون عندما يقترب الغاز من حالة التكثف (التحول لسائل)، أي عند الضغط المرتفع جداً الذي يجبر الجزيئات على الاقتراب، أو الحرارة المنخفضة جداً التي تضعف الطاقة الحركية وتسمح لقوى التجاذب بالظهور.
ما هو الفرق بين الثابت العام للغازات (R) وثابت بولتزمان؟
الثابت العام R يُستخدم عند التعامل مع كميات المادة بالمولات، بينما يُستخدم ثابت بولتزمان k عند التعامل مع الجزيئات الفردية، والعلاقة بينهما هي أن R يساوي ثابت بولتزمان مضروباً في عدد أفوجادرو.




💬 التعليقات