قانون حجم الغاز : أمثلة وتطبيقات
- ما هو الغاز؟ تعريف وحالات المادة
- ما هو قانون حجم الغاز؟ القوانين الأساسية التي تحكم الحجم
- 1. قانون بويل (Boyle’s Law): العلاقة العكسية بين الضغط والحجم
- 2. قانون شارل (Charles’s Law): العلاقة الطردية بين الحجم ودرجة الحرارة
- 3. قانون جاي-لوساك (Gay-Lussac’s Law): العلاقة الطردية بين الضغط ودرجة الحرارة عند ثبات الحجم
- 4. قانون أفوجادرو (Avogadro’s Law): العلاقة الطردية بين الحجم وكمية الغاز
- ما هي القوانين المركبة للغازات؟
- 1. قانون الغاز المجمع (Combined Gas Law)
- 2. قانون الغاز المثالي (Ideal Gas Law)
- ما هي أهمية قوانين الغازات في الحياة اليومية والتطبيقات العملية؟
- في المجال الطبي
- في الصناعة والهندسة
- المصادر والمراجع
- أسئلة شائعة حول قوانين حجم الغاز
- ما الفرق بين قانون بويل وقانون شارل؟
- لماذا يجب استخدام درجة الحرارة المطلقة (الكلفن) في قوانين الغازات؟
- ما هو الحجم المولي للغاز؟
- هل تنطبق قوانين الغازات المثالية على الغازات الحقيقية؟
هل تساءلت يومًا لماذا تنكمش بالونات الهواء عندما تخرج بها إلى الخارج في يوم شديد البرودة؟ أو كيف يعمل محقن الطبيب لسحب الدواء؟ كل هذه الظواهر تخضع لقوانين فيزيائية أنيقة تحكم سلوك الغازات.
في هذا الدليل، سنستكشف معًا قانون حجم الغاز والقوانين الأخرى التي تشرح العلاقة بين الحجم والضغط ودرجة الحرارة وكمية الغاز. سواء كنت طالبًا أو معلمًا أو مجرد فضولي، ستجد هنا شرحًا وافيًا مع أمثلة حياتية وتطبيقات عملية.
ما هو الغاز؟ تعريف وحالات المادة
قبل أن نتعمق في قانون حجم الغاز، دعنا نتعرف على طبيعة الغاز نفسه. الغاز هو إحدى حالات المادة الثلاث الأساسية إلى جانب الصلبة والسائلة.
يتميز الغاز بأن جزيئاته متباعدة جدًا وتتحرك بحرية وعشوائية، وليس له شكل أو حجم ثابت، بل ينتشر ليملأ أي وعاء يوضع فيه. الغازات أقل كثافة وأخف وزنًا من المواد الصلبة والسائلة، ويمكن تمييزها من خلال العديد من الخواص الكيميائية المختلفة كالوزن والقدرة على الامتصاص وغيرها.
لفهم سلوك الغازات، نستخدم أربعة متغيرات أساسية تصف حالتها:
- الضغط (P): القوة التي تؤثر بها جزيئات الغاز على وحدة المساحة من جدار الوعاء. يُقاس بوحدات مثل الباسكال (Pa)، أو الضغط الجوي (atm)، أو المليمتر زئبق (mmHg).
- الحجم (V): الحيز الذي يشغله الغاز، وهو يساوي حجم الوعاء الذي يحتويه. يُقاس باللتر (L) أو المتر المكعب (m³).
- درجة الحرارة (T): مقياس لمتوسط الطاقة الحركية لجزيئات الغاز. في جميع قوانين الغازات، يجب دائمًا استخدام مقياس درجة الحرارة المطلقة (الكلفن – K). للتحويل من الدرجة المئوية إلى الكلفن: K = °C + 273.15.
- كمية الغاز (n): عدد جزيئات الغاز، وعادة ما يُعبر عنها بعدد المولات (mol).
قوانين الغازات هي مجموعة من القوانين التي تصف العلاقة بين هذه المتغيرات الأربعة. القوانين الأساسية التي تركز على الحجم هي: قانون بويل، قانون شارل، قانون جاي-لوساك، وقانون أفوجادرو.
ما هو قانون حجم الغاز؟ القوانين الأساسية التي تحكم الحجم
يُعد مصطلح “قانون حجم الغاز” مصطلحًا جامعًا لمجموعة من القوانين التي تصف كيف يتغير حجم الغاز استجابة للتغيرات في الضغط ودرجة الحرارة وكمية المادة. إليك أهم هذه القوانين:
1. قانون بويل (Boyle’s Law): العلاقة العكسية بين الضغط والحجم
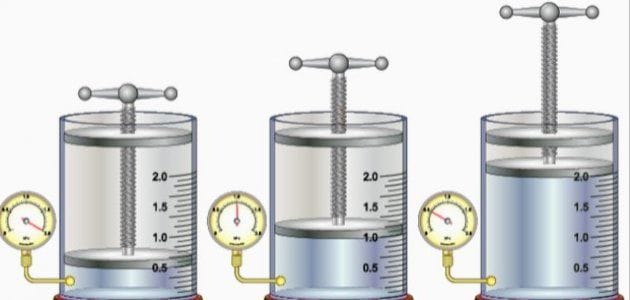
اكتشف العالم روبرت بويل (Robert Boyle) هذا القانون في القرن السابع عشر. ينص قانون بويل على أنه “عند ثبات درجة الحرارة وكمية الغاز، يتناسب حجم الغاز تناسبًا عكسيًا مع ضغطه”. بعبارة أبسط، إذا ضغطت على الغاز (زيادة الضغط)، سيقل حجمه. وإذا سمحت له بالتمدد (تقليل الضغط)، سيزداد حجمه. هذا يعني أن حاصل ضرب الضغط في الحجم يبقى ثابتًا طالما بقيت درجة الحرارة ثابتة.
الصيغة الرياضية لقانون بويل
يمكن التعبير عن قانون بويل بالمعادلة التالية:
- ض × ح = ثابت (عند ثبوت درجة الحرارة وكمية الغاز)
- أو بصيغة أخرى: ض₁ × ح₁ = ض₂ × ح₂
حيث:
- ض₁، ح₁: الضغط والحجم الابتدائيان
- ض₂، ح₂: الضغط والحجم النهائيان
تطبيقات عملية على قانون بويل
من أبرز التطبيقات اليومية لقانون بويل:
- عمل المحقنة (السرنجة): عندما تسد فوهة المحقنة وتضغط على المكبس، فإنك تزيد الضغط على الهواء داخل المحقنة، مما يقلل حجمه. وعند سحب المكبس، يقل الضغط ويزداد حجم الهواء.
- تنفس الإنسان: عند الشهيق، ينقبض الحجاب الحاجز ويزداد حجم الرئتين، مما يقلل الضغط داخلها، فيندفع الهواء إلى الداخل. وعند الزفير، ينعكس الوضع.
- مضخات الهواء: تعتمد مضخات الإطارات والبالونات على مبدأ قانون بويل لدفع الهواء إلى حيز ضيق.
2. قانون شارل (Charles’s Law): العلاقة الطردية بين الحجم ودرجة الحرارة
اكتشف العالم الفرنسي جاك شارل (Jacques Charles) هذا القانون عام 1787، ثم طوره جوزيف لويس جاي-لوساك لاحقًا. ينص قانون شارل على أنه “عند ثبات الضغط وكمية الغاز، يتناسب حجم الغاز تناسبًا طرديًا مع درجة حرارته المطلقة (بالكلفن)”. هذا يعني أنه إذا زادت درجة حرارة الغاز، يتمدد ويزداد حجمه، وإذا انخفضت درجة حرارته، ينكمش ويقل حجمه.
الصيغة الرياضية لقانون شارل
يمكن التعبير عن قانون شارل بالمعادلة التالية:
- ح/د = ثابت (عند ثبوت الضغط)
- أو بصيغة أخرى: ح₁ / د₁ = ح₂ / د₂
حيث:
- ح₁، د₁: الحجم ودرجة الحرارة (بالكلفن) الابتدائيان
- ح₂، د₂: الحجم ودرجة الحرارة (بالكلفن) النهائيان
تطبيقات عملية على قانون شارل
من أبرز التطبيقات اليومية لقانون شارل:
- انكماش البالونات في الطقس البارد: عندما تخرج بالونًا مملوءًا بالهواء إلى الخارج في يوم شديد البرودة، تنخفض درجة حرارته، فيقل حجمه ويبدو منكمشًا.
- ارتفاع بالونات الهواء الساخن: يتم تسخين الهواء داخل البالون، مما يزيد من حجمه ويقلل من كثافته، فيرتفع البالون إلى أعلى.
- قياس درجة الحرارة: تعتمد بعض موازين الحرارة على تمدد السوائل أو الغازات بتغير درجة الحرارة.
3. قانون جاي-لوساك (Gay-Lussac’s Law): العلاقة الطردية بين الضغط ودرجة الحرارة عند ثبات الحجم
ينص قانون جاي-لوساك على أنه “عند ثبات حجم وكمية الغاز، يتناسب ضغط الغاز تناسبًا طرديًا مع درجة حرارته المطلقة”. هذا يعني أنه إذا زادت درجة حرارة الغاز داخل وعاء مغلق (ثابت الحجم)، سيزداد ضغطه. وإذا انخفضت درجة الحرارة، سيقل ضغطه.
الصيغة الرياضية لقانون جاي-لوساك
يمكن التعبير عن قانون جاي-لوساك بالمعادلة التالية:
- ض₁ / د₁ = ض₂ / د₂
حيث:
- ض₁، د₁: الضغط ودرجة الحرارة (بالكلفن) الابتدائيان
- ض₂، د₂: الضغط ودرجة الحرارة (بالكلفن) النهائيان
تطبيقات عملية على قانون جاي-لوساك
من أبرز التطبيقات اليومية لقانون جاي-لوساك:
- علب الأيروسول (البخاخات): تحذّر التعليمات على علب مزيل العرق أو طلاء الشعر من تخزينها في أماكن حارة، لأن ارتفاع درجة الحرارة يزيد من ضغط الغاز داخل العلبة وقد يؤدي إلى انفجارها.
- إطارات السيارات: عند قيادة السيارة لمسافات طويلة، ترتفع درجة حرارة الإطارات، مما يزيد من ضغط الهواء داخلها. لهذا السبب، يُنصح بفحص ضغط الإطارات وهي باردة.
4. قانون أفوجادرو (Avogadro’s Law): العلاقة الطردية بين الحجم وكمية الغاز
ينص قانون أفوجادرو على أنه “عند نفس الظروف من درجة الحرارة والضغط، فإن أحجامًا متساوية من الغازات المختلفة تحتوي على عدد متساوٍ من الجزيئات”. هذا يعني أن حجم الغاز يتناسب طرديًا مع عدد مولاته (أو عدد جزيئاته) عند ثبوت درجة الحرارة والضغط. كما أن الحجم الذي يشغله مول واحد من أي غاز في الظروف القياسية (0°C و 1 atm) هو 22.4 لترًا، وتُعرف هذه القيمة بالحجم المولي للغاز.
الصيغة الرياضية لقانون أفوجادرو
يمكن التعبير عن قانون أفوجادرو بالمعادلة التالية:
- ح / ن = ثابت (عند ثبوت الضغط ودرجة الحرارة)
- أو بصيغة أخرى: ح₁ / ن₁ = ح₂ / ن₂
حيث:
- ح: حجم الغاز
- ن: عدد مولات الغاز
تطبيقات عملية على قانون أفوجادرو
من أبرز التطبيقات العملية لقانون أفوجادرو:
- حساب حجم الغازات في التفاعلات الكيميائية: يمكن استخدام النسب الحجمية للغازات المتفاعلة والناتجة في التفاعلات الكيميائية لتحديد كميات المواد المتفاعلة والناتجة.
- التحليل الوزني للغازات: يمكن تحديد كتلة غاز مجهول من خلال معرفة حجمه في الظروف القياسية.
- صناعة البالونات المملوءة بالهيليوم: معرفة العلاقة بين الحجم وكمية الغاز تساعد في تحديد كمية الهيليوم اللازمة لملء بالون بحجم معين.
ما هي القوانين المركبة للغازات؟
بعد أن تعرفنا على القوانين الأساسية، يمكننا دمجها في قوانين أكثر شمولاً تصف سلوك الغازات بدقة أكبر.
1. قانون الغاز المجمع (Combined Gas Law)
يجمع قانون الغاز المجمع بين القوانين الثلاثة الأولى: قانون بويل، وقانون شارل، وقانون جاي-لوساك. ينص هذا القانون على أن النسبة بين حاصل ضرب الضغط في الحجم ودرجة الحرارة هي مقدار ثابت. يمكن استخدام هذا القانون لمقارنة تغيرات المادة عند ظروف مختلفة.
الصيغة الرياضية لقانون الغاز المجمع:
- ض₁ × ح₁ / د₁ = ض₂ × ح₂ / د₂
2. قانون الغاز المثالي (Ideal Gas Law)
يعد قانون الغاز المثالي من أهم القوانين في الكيمياء والفيزياء. يجمع هذا القانون بين جميع القوانين السابقة (بويل، شارل، جاي-لوساك، وأفوجادرو) ليعطي علاقة شاملة تربط جميع المتغيرات الأربعة: الضغط والحجم ودرجة الحرارة وعدد المولات.
الصيغة الرياضية لقانون الغاز المثالي:
- ض × ح = ن × ث × د
حيث:
- ض: الضغط
- ح: الحجم
- ن: عدد مولات الغاز
- ث: ثابت الغاز العام (Universal Gas Constant)، قيمته 0.0821 لتر·ضغط جوي·مول⁻¹·كلفن⁻¹ أو 8.314 جول·مول⁻¹·كلفن⁻¹
- د: درجة الحرارة المطلقة (بالكلفن)
يفترض قانون الغاز المثالي أن جزيئات الغاز هي مجرد نقاط لا تشغل حيزًا ولا تتفاعل مع بعضها البعض. على الرغم من عدم وجود غاز مثالي حقيقي، إلا أن هذا القانون يصف سلوك معظم الغازات الحقيقية بدقة مقبولة في الظروف العادية (ضغوط منخفضة ودرجات حرارة مرتفعة).
يمكنك استخدام معادلة الغاز المثالي لحساب أي من المتغيرات الأربعة إذا كنت تعرف الثلاثة الأخرى. على سبيل المثال، يمكن حساب كتلة غاز معين من خلال معرفة حجمه وضغطه ودرجة حرارته، باستخدام العلاقة بين عدد المولات والكتلة المولية للغاز. للمزيد عن مفاهيم الكتلة المولية والحسابات الكيميائية، يمكنك الاطلاع على مقالنا عن الكتلة المولية.
ما هي أهمية قوانين الغازات في الحياة اليومية والتطبيقات العملية؟
لقوانين الغازات أهمية بالغة في العديد من المجالات العلمية والصناعية والطبية، ومنها:
في المجال الطبي
تُستخدم قوانين الغازات في تفسير آلية عمل العديد من الأدوية والعمليات الحيوية في الجسم. على سبيل المثال، يستخدم قانون هنري (الذي يصف ذوبان الغازات في السوائل) في فهم كيفية انتقال الأكسجين وثاني أكسيد الكربون في الدم. كما تُستخدم قوانين الغازات في تصميم أجهزة التنفس الصناعي وأجهزة التخدير.
في الصناعة والهندسة
تُستخدم قوانين الغازات في تصميم محطات توليد الطاقة، والمحركات، والمكابس، ومكيفات الهواء، وأجهزة التبريد. كما أنها أساسية في الصناعات الكيميائية لتقدير كميات الغازات الداخلة والخارجة من المفاعلات.
إذا كنت مهتمًا بشراء المواد الكيميائية والغازات المستخدمة في التطبيقات الصناعية والمختبرية، يمكنك زيارة متجر عالم الكيماويات للمواد الخام والكيماويات.
المصادر والمراجع
اعتمدت في هذا الشرح على مصادر علمية موثوقة:
- موقع موضوع – “قانون حجم الغاز” – تعريف الغاز وقوانين بويل وشارل وجاي-لوساك – تاريخ الاطلاع: مارس 2026 – https://mawdoo3.com/قانون_حجم_الغاز
- موسوعة Britannica – “Avogadro’s law” – تعريف قانون أفوجادرو والحجم المولي – تاريخ الاطلاع: مارس 2026 – https://www.britannica.com/science/Avogadros-law
- موسوعة Britannica – “Ideal gas law” – تعريف قانون الغاز المثالي – تاريخ الاطلاع: مارس 2026 – https://www.britannica.com/science/ideal-gas-law
- موقع عالم الكيماويات – “قوانين الغازات: 7 قوانين أساسية” – شرح مفصل لقوانين الغازات وتطبيقاتها – تاريخ الاطلاع: مارس 2026 – https://chemicalsmed.com/قوانين-الغازات/
- معهد ديفيدسون – “قوانين الغازات المثاليّة” – شرح المتغيرات الأربعة وافتراضات الغاز المثالي – تاريخ الاطلاع: مارس 2026 – https://davidson.org.il/read-experience/ar/maagarmada-ar/قوانين-الغازات-المثاليّة/
أسئلة شائعة حول قوانين حجم الغاز
ما الفرق بين قانون بويل وقانون شارل؟
قانون بويل يصف العلاقة بين الضغط والحجم عند ثبوت درجة الحرارة، وهي علاقة عكسية (كلما زاد الضغط قل الحجم). أما قانون شارل فيصف العلاقة بين الحجم ودرجة الحرارة عند ثبوت الضغط، وهي علاقة طردية (كلما زادت درجة الحرارة زاد الحجم).
لماذا يجب استخدام درجة الحرارة المطلقة (الكلفن) في قوانين الغازات؟
لأن درجة الحرارة المطلقة تتناسب طرديًا مع متوسط الطاقة الحركية لجزيئات الغاز، بينما لا توجد هذه العلاقة في الدرجات المئوية. كما أن استخدام الكلفن يتجنب القيم السالبة التي لا معنى لها في سياق قوانين الغازات (لا يمكن أن يكون الحجم أو الضغط سالبًا).
ما هو الحجم المولي للغاز؟
الحجم المولي للغاز هو الحجم الذي يشغله مول واحد من أي غاز في الظروف القياسية من درجة الحرارة والضغط (STP: 0°C و 1 atm)، ويساوي 22.4 لترًا. هذه القيمة ثابتة لجميع الغازات بموجب قانون أفوجادرو.
هل تنطبق قوانين الغازات المثالية على الغازات الحقيقية؟
قوانين الغازات المثالية هي تقريب جيد لسلوك معظم الغازات الحقيقية في الظروف العادية (ضغوط منخفضة ودرجات حرارة مرتفعة). لكن عند الضغوط العالية جدًا أو درجات الحرارة المنخفضة جدًا (قرب نقطة التكثف)، تختلف سلوك الغازات الحقيقية عن النموذج المثالي بسبب قوى التجاذب بين الجزيئات وحجمها الفعلي. في هذه الحالات، تُستخدم معادلات حالة أكثر تعقيدًا مثل معادلة فان دير فالس.




💬 التعليقات