قانون حفظ الكتلة : المبدأ، أهميته، وأمثلة عليه
- ما هو قانون حفظ الكتلة؟
- من هو مكتشف قانون حفظ الكتلة؟
- لماذا يعتبر قانون حفظ الكتلة مهماً؟
- أمثلة على قانون حفظ الكتلة في الحياة اليومية
- مثال 1: تفاعل احتراق الميثان (الغاز الطبيعي)
- مثال 2: تجربة الخل وصودا الخبز في بالون مغلق
- مثال 3: احتراق شمعة في وعاء مغلق
- المصادر والمراجع
- أسئلة شائعة حول قانون حفظ الكتلة
- هل ينطبق قانون حفظ الكتلة في التفاعلات النووية؟
- كيف أستخدم قانون حفظ الكتلة لموازنة معادلة كيميائية؟
- هل توجد استثناءات لقانون حفظ الكتلة في الكيمياء التقليدية؟
هل تساءلت يوماً لماذا عند حرق قطعة خشب، يبدو أن كتلتها تتناقص بينما يزداد الرماد والدخان؟ أو لماذا يكون مجموع كتل المواد الداخلة في تفاعل كيميائي مساوياً تماماً لمجموع كتل المواد الخارجة منه؟
الإجابة تكمن في أحد أهم القوانين في الكيمياء: قانون حفظ الكتلة (Law of Conservation of Mass). في هذا الدليل، سنتعرف على هذا القانون العبقري، وأهميته، ونقدم أمثلة تطبيقية لفهمه بشكل أفضل.
ما هو قانون حفظ الكتلة؟
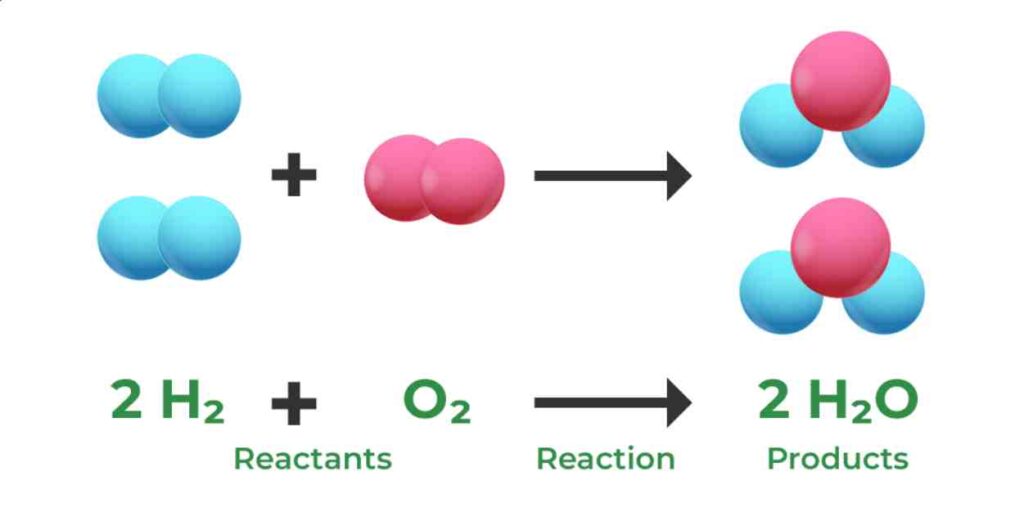
قانون حفظ الكتلة، الذي يُعرف أيضاً بقانون حفظ المادة، هو مبدأ أساسي في الكيمياء والفيزياء ينص على أن الكتلة لا تُفنى ولا تُستحدث من العدم، بل تتحول من شكل إلى آخر.
بمعنى آخر، في أي نظام مغلق (لا يسمح بتبادل المادة مع المحيط)، تبقى الكتلة الإجمالية للنظام ثابتة مهما حدث من تغيرات كيميائية أو فيزيائية. هذا يعني أن مجموع كتل المواد المتفاعلة (المتفاعلات) في أي تفاعل كيميائي يساوي دائماً مجموع كتل المواد الناتجة (النواتج). للمزيد عن أساسيات التفاعلات الكيميائية، يمكنك الاطلاع على مفهوم التفاعلات الكيميائية.
من هو مكتشف قانون حفظ الكتلة؟
على الرغم من أن الفكرة كانت مطروحة بشكل بدائي عند بعض العلماء القدماء، إلا أن العالم الفرنسي أنطوان لافوازييه (Antoine Lavoisier) هو من وضع القانون بصيغته الحديثة والمعروفة في أواخر القرن الثامن عشر (حوالي 1785).
أجرى لافوازييه سلسلة من التجارب الدقيقة التي قاس فيها بدقة كتل المواد قبل وبعد التفاعلات الكيميائية في أوعية مغلقة، وأثبت أن الكتلة الكلية تبقى ثابتة. لقد دحض بذلك نظرية “الفلوجستون” السائدة آنذاك، والتي فسرت الاحتراق بشكل خاطئ. لهذا السبب، يُعتبر لافوازييه أبو الكيمياء الحديثة.
لماذا يعتبر قانون حفظ الكتلة مهماً؟
تكمن أهمية قانون حفظ الكتلة في كونه حجر الزاوية للكيمياء الحديثة:
- أساس المعادلات الكيميائية: يضمن صحة المعادلات الكيميائية من خلال موازنة عدد ذرات كل عنصر في طرفي المعادلة (المتفاعلات والنواتج).
- حسابات التفاعلات الكيميائية (القياس الكيميائي – Stoichiometry): يسمح للكيميائيين بحساب كميات المواد المتفاعلة اللازمة والمواد الناتجة المتوقعة بدقة.
- تطبيقات عملية متعددة: يستخدم في مجالات متعددة مثل تصميم المفاعلات الكيميائية، وفي الصناعات الدوائية والغذائية، وفي مراقبة التلوث البيئي.
أمثلة على قانون حفظ الكتلة في الحياة اليومية
دعنا نرى كيف ينطبق هذا القانون على تفاعلات نعرفها:
مثال 1: تفاعل احتراق الميثان (الغاز الطبيعي)
تفاعل الميثان مع الأكسجين لإنتاج ثاني أكسيد الكربون والماء: CH₄ + 2O₂ → CO₂ + 2H₂O. إذا حسبنا كتل الذرات:
- كتلة المتفاعلات: 12 (كربون) + 4 (هيدروجين) + 64 (أكسجين) = 80 وحدة كتلة.
- كتلة النواتج: 12 (كربون) + 32 (أكسجين) + 4 (هيدروجين) + 32 (أكسجين) = 80 وحدة كتلة.
الكتلة محفوظة تماماً.
مثال 2: تجربة الخل وصودا الخبز في بالون مغلق
إذا وضعت بيكربونات الصوديوم (صودا الخبز) والخل في زجاجة وأغلقت فوهتها ببالون، سيحدث تفاعل ينتج غاز ثاني أكسيد الكربون فينفخ البالون. إذا قمت بوزن الزجاجة والبالون والمحتويات قبل التفاعل وبعده، ستجد أن الوزن لم يتغير. فبالرغم من تكون غاز جديد، إلا أن كتلته محصورة داخل النظام المغلق، مما يثبت حفظ الكتلة. للمزيد عن تجارب منزلية مشابهة، يمكنك قراءة طرق صنع منظف أرضيات منزلي حيث تستخدم هذه المواد.
مثال 3: احتراق شمعة في وعاء مغلق
إذا أحرقت شمعة داخل وعاء زجاجي مغلق بإحكام، فإن وزن الوعاء ومحتوياته يبقى ثابتاً. يتحول الشمع (الكربون والهيدروجين) إلى ثاني أكسيد الكربون وبخار الماء، لكن جميع الذرات تبقى محصورة داخل الوعاء.
إذا كنت مهتماً بتجارب كيميائية دقيقة تحتاج إلى مواد عالية النقاء، يمكنك زيارة متجر عالم الكيماويات للمواد الخام والكيماويات لتوفير احتياجاتك.
المصادر والمراجع
اعتمدت في هذا الدليل على مصادر علمية موثوقة:
- Nature Education – “The Conservation of Mass” – تاريخ الاطلاع: أبريل 2026 – https://www.nature.com/scitable/knowledge/library/the-conservation-of-mass-17395478
- Chemistry LibreTexts – “3.7: Conservation of Mass: There is No New Matter” – تاريخ الاطلاع: أبريل 2026 – https://chem.libretexts.org/…/3.07%3A_Conservation_of_Mass%3A_There_is_No_New_Matter
- Study.com – “The Law of Conservation of Mass: Definition, Equation & Examples” – تاريخ الاطلاع: أبريل 2026 – https://study.com/academy/lesson/the-law-of-conservation-of-mass-definition-equation-examples.html
أسئلة شائعة حول قانون حفظ الكتلة
هل ينطبق قانون حفظ الكتلة في التفاعلات النووية؟
لا، لا ينطبق قانون حفظ الكتلة بالمعنى الكلاسيكي على التفاعلات النووية. في التفاعلات النووية (كانشطار أو اندماج)، يتم تحويل جزء صغير من الكتلة إلى طاقة هائلة وفقاً لمعادلة أينشتاين E=mc². هنا، يتم حفظ الكتلة والطاقة معاً (حفظ الطاقة الكتلية)، وليس الكتلة وحدها.
كيف أستخدم قانون حفظ الكتلة لموازنة معادلة كيميائية؟
عند موازنة معادلة، تأكد أن عدد ذرات كل عنصر في طرف المتفاعلات يساوي عددها في طرف النواتج. يمكنك إضافة معاملات (أرقام قبل الصيغ الكيميائية) لتحقيق ذلك. هذا يضمن أن الكتلة الكلية محفوظة.
هل توجد استثناءات لقانون حفظ الكتلة في الكيمياء التقليدية؟
في الكيمياء التقليدية (غير النووية)، لا توجد استثناءات عملية. القياسات الدقيقة جداً قد تظهر فروقاً طفيفة جداً ناتجة عن حدود دقة الأجهزة، لكن المبدأ الأساسي صحيح تماماً. في بعض التفاعلات التي تتضمن إطلاق غازات، إذا لم يكن النظام مغلقاً، قد يبدو أن الكتلة قد نقصت، لكن الغاز المنطلق له كتلة محسوبة ضمن النظام المغلق.




💬 التعليقات