قوة الحمض والقاعدة : الفرق بين القوي والضعيف
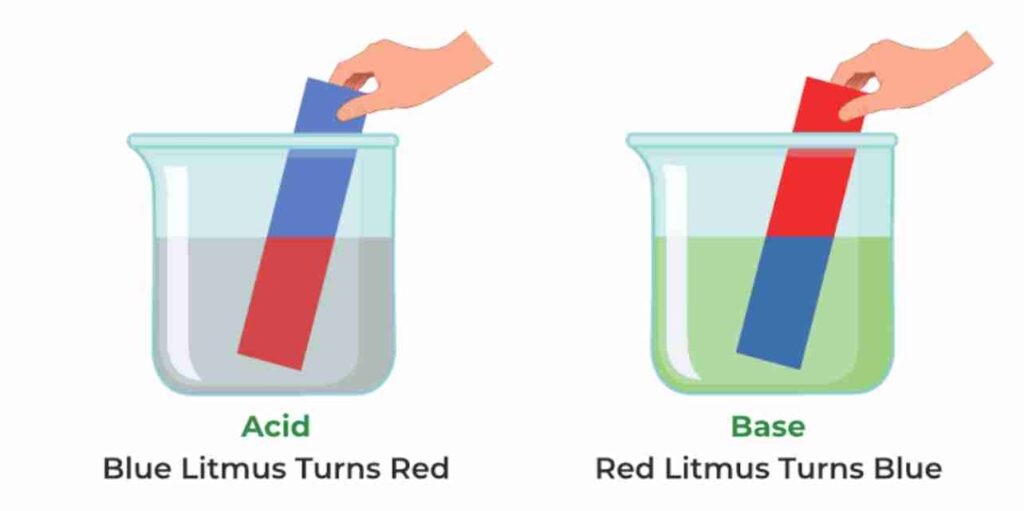
- المصطلحات المرتبطة بقوة الحمض والقاعدة
- قوة وخصائص الحمض
- أولاً: الحمض القوي (Strong Acid)
- ثانياً: الحمض الضعيف (Weak Acid)
- قوة وخصائص القاعدة
- أولاً: القاعدة القوية (Strong Base)
- ثانياً: القاعدة الضعيفة (Weak Base)
- جدول مقارنة سريع: القوي مقابل الضعيف
- الأسئلة الشائعة
- هل الحمض القوي دائماً خطر؟
- كيف أعرف إذا كان الحمض قوياً أم ضعيفاً بدون تجربة؟
- هل القواعد القوية تسبب حروقاً مثل الأحماض؟
- ما هو أقوى حمض معروف؟
- هل يمكن تحويل حمض ضعيف إلى قوي؟
- المصادر والمراجع
المصطلحات المرتبطة بقوة الحمض والقاعدة
لنفهم قوة الحمض أو القاعدة، يجب أن نعرف بعض المصطلحات الأساسية:
- التفكك (Dissociation): هو انفصال جزيء الحمض أو القاعدة إلى أيوناته الموجبة والسالبة عند ذوبانه في الماء.
- ثابت التفكك الحمضي (Ka): قيمة رقمية تعبر عن مدى ميل الحمض للتفكك. كلما زادت Ka، زادت قوة الحمض.
- ثابت التفكك القاعدي (Kb): نفس الفكرة ولكن للقواعد. كلما زادت Kb، زادت قوة القاعدة.
- pKa و pKb: هما اللوغاريتم السالب لـ Ka و Kb. كلما صغرت قيمة pKa، زادت قوة الحمض. (علاقة عكسية).
هذه القيم الثابتة هي ما يستخدمها الكيميائيون لمقارنة القوة بدقة، بدلاً من الاعتماد على التوصيفات النوعية فقط.
قوة وخصائص الحمض
تقسم الأحماض إلى نوعين رئيسيين حسب قوتها: أحماض قوية وأحماض ضعيفة.
أولاً: الحمض القوي (Strong Acid)
هو حمض يتفكك بشكل كامل تقريباً (100%) في الماء. يعني ذلك أن كل جزيئات الحمض تتحول إلى أيونات H⁺ وأيونات سالبة. لا يبقى أي جزيئات غير متفككة. أمثلة شهيرة: حمض الهيدروكلوريك (HCl) الموجود في المعدة، وحمض الكبريتيك (H₂SO₄) المستخدم في البطاريات، وحمض النيتريك (HNO₃).
خصائص الأحماض القوية:
- موصلية كهربائية عالية جداً لأنها تعطي الكثير من الأيونات الحرة.
- تفاعلاتها سريعة وعنيفة مع المعادن والقواعد.
- تآكل شديد للجلد والأنسجة.
- قيم pKa لها سالبة (أقل من صفر).
ثانياً: الحمض الضعيف (Weak Acid)
هو حمض يتفكك بشكل جزئي فقط في الماء. معظم جزيئاته تبقى سليمة، وقليل منها فقط يتحول إلى أيونات. أمثلة: حمض الخليك (CH₃COOH) الموجود في الخل، وحمض الستريك في الليمون، وحمض الكربونيك في المشروبات الغازية.
خصائص الأحماض الضعيفة:
- موصلية كهربائية منخفضة نسبياً.
- تفاعلاتها أبطأ وأقل عنفاً.
- توجد في الطعام والطبيعة بكثرة.
- قيم pKa لها موجبة (عادة بين 2 و 14).
مهم جداً: لا تخلط بين “القوة” و”التركيز”. حمض ضعيف لكن بتركيز عالٍ قد يكون خطيراً، وحمض قوي لكن بتركيز منخفض جداً قد يكون آمناً نسبياً.
قوة وخصائص القاعدة
نفس المبدأ ينطبق على القواعد، لكن مع أيونات الهيدروكسيد (OH⁻).
أولاً: القاعدة القوية (Strong Base)
تتفكك بشكل كامل في الماء لإنتاج أيونات OH⁻. أمثلة: هيدروكسيد الصوديوم (NaOH) الموجود في مزيلات انسداد البالوعات، وهيدروكسيد البوتاسيوم (KOH)، وهيدروكسيد الكالسيوم (الجير المطفأ).
خصائص القواعد القوية:
- موصلية كهربائية عالية.
- تآكل شديد للجلد والأنسجة (حرق كيميائي).
- ملمس صابوني زلق جداً.
- تتفاعل بعنف مع الأحماض.
ثانياً: القاعدة الضعيفة (Weak Base)
تتفكك بشكل جزئي فقط في الماء. أمثلة: الأمونيا (NH₃) المستخدمة في منظفات الزجاج، وكربونات الصوديوم (صودا الخبز)، والأمينات العضوية الموجودة في البروتينات.
خصائص القواعد الضعيفة:
- موصلية كهربائية منخفضة.
- أقل تآكلاً من القواعد القوية.
- توجد في العديد من المنتجات المنزلية والبيولوجية.
إذا كنت مهتماً بكيمياء المركبات العضوية التي تحتوي على مجموعات حمضية وقاعدية، يمكنك قراءة مقالنا عن المركبات الحلقية غير المتجانسة.
جدول مقارنة سريع: القوي مقابل الضعيف
| الخاصية | حمض/قاعدة قوي | حمض/قاعدة ضعيف |
|---|---|---|
| درجة التفكك في الماء | كاملة (~100%) | جزئية (<10%) |
| ثابت التفكك (Ka/Kb) | كبير جداً (>1) | صغير (<1) |
| pKa / pKb | أقل من صفر (سلبي) | موجب (غالباً >0) |
| مثال حمض | HCl (حمض الهيدروكلوريك) | CH₃COOH (حمض الخليك) |
| مثال قاعدة | NaOH (هيدروكسيد الصوديوم) | NH₃ (الأمونيا) |
موقع Britannica يقدم شرحاً موسعاً عن الأحماض والقواعد وتصنيفاتها.
خلاصة: قوة الحمض أو القاعدة تحددها قدرتها الطبيعية على التفكك، وليس تركيزها في المحلول. الأحماض والقوية القوية خطيرة وفعالة، بينما الضعيفة منها أكثر أماناً وتنتشر في الطبيعة والطعام.
الأسئلة الشائعة
هل الحمض القوي دائماً خطر؟
ليس بالضرورة. الخطر يعتمد على التركيز والمدة. حمض الهيدروكلوريك بتركيز 0.1% موجود في المعدة ويساعد على الهضم دون ضرر. لكنه يصبح خطيراً بتركيزات عالية.
كيف أعرف إذا كان الحمض قوياً أم ضعيفاً بدون تجربة؟
يمكنك معرفة ذلك من خلال الجداول المعروفة لقيم pKa. الأحماض القوية لها pKa سالب (مثل HCl: pKa ≈ -7). الأحماض الضعيفة لها pKa موجب (حمض الخليك: pKa ≈ 4.76).
هل القواعد القوية تسبب حروقاً مثل الأحماض؟
نعم، القواعد القوية (مثل هيدروكسيد الصوديوم) تسبب حروقاً كيميائية شديدة قد تكون أعمق وأصعب في العلاج من حروق الأحماض لأنها تدمر البروتينات والدهون فوراً.
ما هو أقوى حمض معروف؟
أقوى الأحماض المعروفة هي “أحماض فائقة القوة” مثل حمض الفلوروأنتيمونيك (H₂FSbF₆)، وهو أقوى بمليارات المرات من حمض الكبريتيك المركز. لكنه لا يستخدم في الحياة اليومية أبداً.
هل يمكن تحويل حمض ضعيف إلى قوي؟
لا يمكن تغيير قوة الحمض الجوهرية (ثابت التفكك Ka) لأنها خاصية فيزيائية كيميائية ثابتة لكل مادة. لكن يمكن زيادة تركيزه أو درجة حرارته لتسريع التفاعل.




💬 التعليقات