مستويات طاقة ذرة الهيدروجين
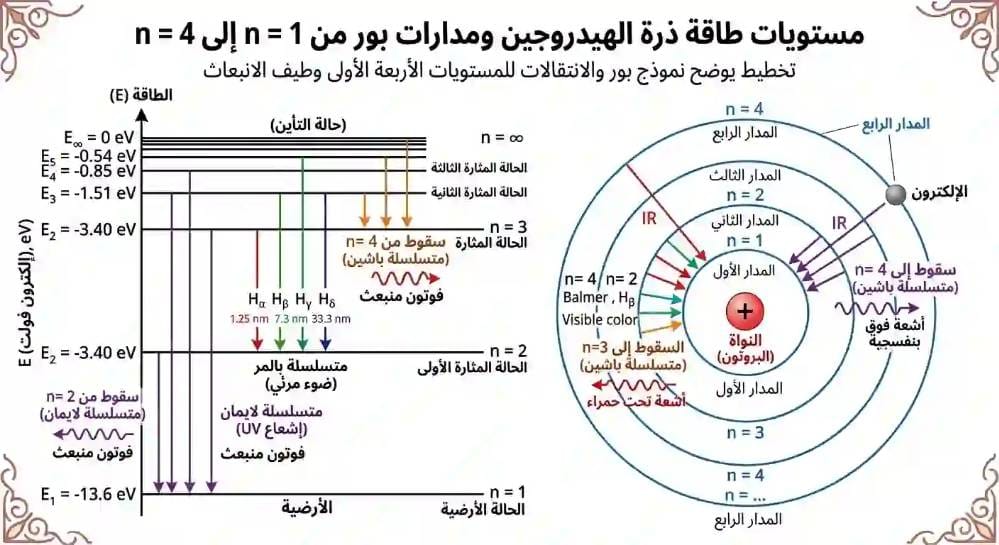
- نموذج بور ومفهوم مستويات طاقة ذرة الهيدروجين
- فرضية التكميم: لماذا لا ينهار الإلكترون في النواة؟
- نصف القطر المسموح به (نصف قطر بور)
- معادلة مستويات الطاقة في ذرة الهيدروجين: \( E_n = -\frac{13.6}{n^2} \text{ eV} \)
- معنى الإشارة السالبة (طاقة الربط)
- تفسير العدد الكمي الرئيسي (n) وأهميته
- كيف تنتج مستويات الطاقة خطوط الطيف؟
- الامتصاص مقابل الانبعاث: الفرق بين القفزات الصاعدة والهابطة
- سلسلة بالمر (Balmer Series): لماذا نرى الضوء المرئي؟
- سلسلة ليمان (Lyman) والأشعة فوق البنفسجية
- من النظرية إلى التطبيق: استخدامات مستويات الطاقة في عصرنا
- الليزر (Laser)
- التحليل الطيفي وتحديد تركيب النجوم
- الخلاصة: أساس فيزياء الكم
عندما تنظر إلى السماء ليلاً، ترى أطيافًا ضوئية تخبرك عن عناصر النجوم البعيدة. كيف يمكن لذرة واحدة، هي ذرة الهيدروجين، أن تكون مفتاح فهم هذا الكون؟ السر يكمن في ما يُعرف بـ مستويات طاقة ذرة الهيدروجين. فالإلكترون في ذرة الهيدروجين لا يدور عشوائيًا، بل يقتصر على مدارات محددة وطاقات محددة بدقة. هذا المبدأ الذي وضعه نيلز بور قبل قرن من الزمان لا يزال حجر الزاوية في فيزياء الكم وتطبيقاتها الحديثة.
في هذا الدليل الشامل حول مستويات طاقة ذرة الهيدروجين، سنأخذك في رحلة لفهم هذه المستويات من جذورها في نموذج بور، إلى معادلتها الرياضية، ثم انتقالات الإلكترون التي تنتج الأطياف، وأخيرًا التطبيقات العملية التي غيرت عالمنا.
نموذج بور ومفهوم مستويات طاقة ذرة الهيدروجين
عندما حاول الفيزيائيون في أوائل القرن العشرين فهم الذرة، واجهوا مفارقة: وفقًا للفيزياء الكلاسيكية، كان من المفترض أن يفقد الإلكترون المشحون طاقته باستمرار ويسقط في النواة خلال أجزاء من الثانية. لكن الذرات مستقرة! هنا جاء نيلز بور بفكرته الثورية التي أرست الأساس لفهم مستويات طاقة ذرة الهيدروجين.
فرضية التكميم: لماذا لا ينهار الإلكترون في النواة؟
افترض بور أن الإلكترون لا يمكنه التواجد إلا في مدارات محددة (يطلق عليها حالات طاقة ثابتة) دون أن يشع طاقة. هذه المدارات تتوافق مع أعداد صحيحة تُسمى العدد الكمي الرئيسي ( n ). الإلكترون في هذه المدارات لا يفقد طاقته، ولا ينتقل بينها إلا عندما يمتص أو يصدر كمية محددة من الطاقة (فوتونًا). هذا التكميم هو جوهر مستويات طاقة ذرة الهيدروجين.
نصف القطر المسموح به (نصف قطر بور)
أصغر مدار مسموح هو ( n=1 )، ويبلغ نصف قطره 0.529 أنغستروم، ويُعرف بنصف قطر بور. المدارات الأكبر (n=2,3,4…) تكون أبعد عن النواة. هذا التكميم المكاني هو أول كسر مع النظرة الكلاسيكية.
الشكل 1: رسم توضيحي لمدارات بور في ذرة الهيدروجين، مع إظهار مستويات الطاقة n=1,2,3,4 وأحجامها النسبية.
معادلة مستويات الطاقة في ذرة الهيدروجين: \( E_n = -\frac{13.6}{n^2} \text{ eV} \)
اللغة الرياضية لهذا التكميم بسيطة وأنيقة. طاقة الإلكترون في المستوى ( n ) تعطى بالعلاقة التي تمثل الأساس الرياضي لمستويات طاقة ذرة الهيدروجين:
\[ E_n = -\frac{13.6}{n^2} \ \text{إلكترون فولت (eV)} \]
حيث ( n = 1, 2, 3, \dots ) هو العدد الكمي الرئيسي.
معنى الإشارة السالبة (طاقة الربط)
الإشارة السالبة تعني أن الإلكترون مرتبط بالنواة. لكي نحرره (نتأين الذرة) نحتاج إلى إمداده بطاقة موجبة مقدارها ( 13.6 \ \text{eV} ) عندما يكون في المستوى الأرضي ( n=1 ). كلما زاد ( n )، أصبحت الطاقة أقل سالبية، أي أن الإلكترون أصبح أقل ارتباطًا، حتى عندما ( n \to \infty ) تصبح الطاقة صفرًا ويصبح الإلكترون حرًا. هذه السلم المتقطع هو ما يميز مستويات طاقة ذرة الهيدروجين.
تفسير العدد الكمي الرئيسي (n) وأهميته
( n ) لا يحدد الطاقة فقط، بل أيضًا متوسط بعد الإلكترون عن النواة. المستوى ( n=1 ) يسمى المستوى الأرضي (حالة الطاقة الأدنى). المستويات الأعلى (( n=2,3,\dots )) تسمى مستويات مثارة. هذه المستويات المتقطعة هي التي تعطي الذرة هويتها الطيفية الفريدة.
كيف تنتج مستويات الطاقة خطوط الطيف؟
الذرات تتفاعل مع الضوء من خلال انتقالات الإلكترون. عندما يمتص الإلكترون فوتونًا طاقته تساوي تمامًا الفرق بين مستويين، يقفز إلى مستوى أعلى (إثارة). وعندما يعود تلقائيًا إلى مستوى أقل، ينبعث فوتون بنفس فرق الطاقة. هذه الظاهرة تفسر الأطياف الذرية بناءً على مستويات طاقة ذرة الهيدروجين.
الامتصاص مقابل الانبعاث: الفرق بين القفزات الصاعدة والهابطة
- الامتصاص: إلكترون في مستوى منخفض يمتص فوتونًا ويرتفع إلى مستوى أعلى. نرى ذلك في الأطياف خطوطًا مظلمة (خطوط فراونهوفر).
- الانبعاث: إلكترون في مستوى عالٍ (مثار) يهبط إلى مستوى أقل، ويصدر فوتونًا. نرى ذلك خطوطًا لامعة في الطيف.
سلسلة بالمر (Balmer Series): لماذا نرى الضوء المرئي؟
الانتقالات التي تنتهي عند ( n=2 ) تشكل سلسلة بالمر. هذه الانتقالات تصدر فوتونات في المنطقة المرئية من الطيف. أشهرها خط ( H_\alpha ) الناتج عن الانتقال من ( n=3 ) إلى ( n=2 )، وهو ذو لون أحمر مميز، ويُستخدم في دراسة السدم والنجوم.
سلسلة ليمان (Lyman) والأشعة فوق البنفسجية
الانتقالات التي تنتهي عند ( n=1 ) (المستوى الأرضي) تصدر فوتونات في منطقة الأشعة فوق البنفسجية، ولا تُرى بالعين المجردة. هذه السلسلة تحمل طاقات عالية وتُستخدم في دراسة البلازما والنجوم الساخنة.
الشكل 2: رسم بياني يوضح انتقالات الإلكترون بين مستويات طاقة ذرة الهيدروجين n=1,2,3,4 مع خطوط الطيف الناتجة في سلسلتي ليمان وبالمر.
من النظرية إلى التطبيق: استخدامات مستويات الطاقة في عصرنا
ما بدا كفضول علمي في بدايات القرن العشرين تحول إلى أساس لتقنيات لا غنى عنها اليوم. ففهم مستويات طاقة ذرة الهيدروجين مهد الطريق لعلم الليزر والتحليل الطيفي الحديث.
الليزر (Laser)
يعتمد عمل الليزر على الانبعاث المحفز بين مستويات الطاقة الذرية. فهم مستويات الطاقة في الهيدروجين ساعد في تطوير أنواع عديدة من الليزر المستخدم في الجراحة والاتصالات والصناعة.
التحليل الطيفي وتحديد تركيب النجوم
كل عنصر له بصمة طيفية فريدة. عندما نرى خطوط بالمر في ضوء نجم بعيد، نعرف أن هذا النجم يحتوي على هيدروجين. بل ويمكننا تحديد درجة حرارته وكثافته من شكل تلك الخطوط. بهذه الطريقة عرف العلماء أن الكون يتكون من 75% هيدروجين، وذلك بفضل دراسة مستويات طاقة ذرة الهيدروجين.
الخلاصة: أساس فيزياء الكم
مستويات طاقة ذرة الهيدروجين ليست مجرد معادلة في كتاب الفيزياء؛ إنها النموذج الأول الذي أظهر للعالم أن الطاقة على المستوى الذري مكممة وليست مستمرة. هذا المفهوم هو بوابة فهم العالم الكمي، من الإلكترونيات الدقيقة إلى الطاقة النووية.
هل كان لديك فضول يومًا حول كيف تعرف العلماء تكوين النجوم البعيدة؟ شاركنا رأيك في قسم التعليقات، وأخبرنا أي تطبيق من تطبيقات مستويات الطاقة أثار اهتمامك أكثر.
مصادر موثوقة (روابط خارجية):
– NIST Atomic Spectra Database – قاعدة بيانات معتمدة لخطوط الطيف الذري.
– HyperPhysics: Hydrogen Energy Levels – شرح تفصيلي من جامعة ولاية جورجيا.




💬 التعليقات