تأين الماء : مفهومه ، أهميته
- ما هو تأين الماء؟
- ما هو ثابت تأين الماء (Kw)؟
- مثال لتوضيح تأين الماء
- لماذا يعتبر تأين الماء مهماً في جسم الإنسان؟
- الأسئلة الشائعة
- هل تأين الماء يحدث فقط في الماء النقي؟
- كيف تؤثر درجة الحرارة على تأين الماء و Kw؟
- لماذا نستخدم Kw بدلاً من دراسة تفاعل التأين مباشرة؟
- هل يمكن أن يتأين الماء في الحالة الصلبة (الثلج) أو الغازية (البخار)؟
- كيف يرتبط مفهوم Kw بالرقم الهيدروجيني pH؟
- المصادر والمراجع
ما هو تأين الماء؟
تأين الماء (أو التأين الذاتي للماء) هو تفاعل كيميائي تلقائي يحدث بين جزيئين من الماء، حيث يتبرع أحدهما بأيون هيدروجين (بروتون) للآخر. ينتج عن هذا التفاعل أيون الهيدرونيوم الموجب (H₃O⁺) وأيون الهيدروكسيد السالب (OH⁻).
المعادلة الكيميائية التي تصف هذه العملية هي: 2H₂O(l) ⇌ H₃O⁺(aq) + OH⁻(aq). هذا التفاعل في حالة توازن ديناميكي، حيث تتشكل الأيونات وتعادل في نفس الوقت.
ما هو ثابت تأين الماء (Kw)؟
للتعبير عن هذا التوازن كمياً، يستخدم الكيميائيون “ثابت تأين الماء” ويرمز له بالرمز Kw. وهو يساوي حاصل ضرب تركيز أيون الهيدرونيوم في تركيز أيون الهيدروكسيد في الماء النقي عند درجة حرارة معينة.
الصيغة الرياضية هي: Kw = [H₃O⁺] [OH⁻]. في درجة حرارة 25 درجة مئوية، تبلغ قيمة Kw حوالي 1.0 × 10⁻¹⁴. هذا الرقم الصغير جداً يخبرنا أن الماء النقي يتأين بدرجة ضئيلة جداً.
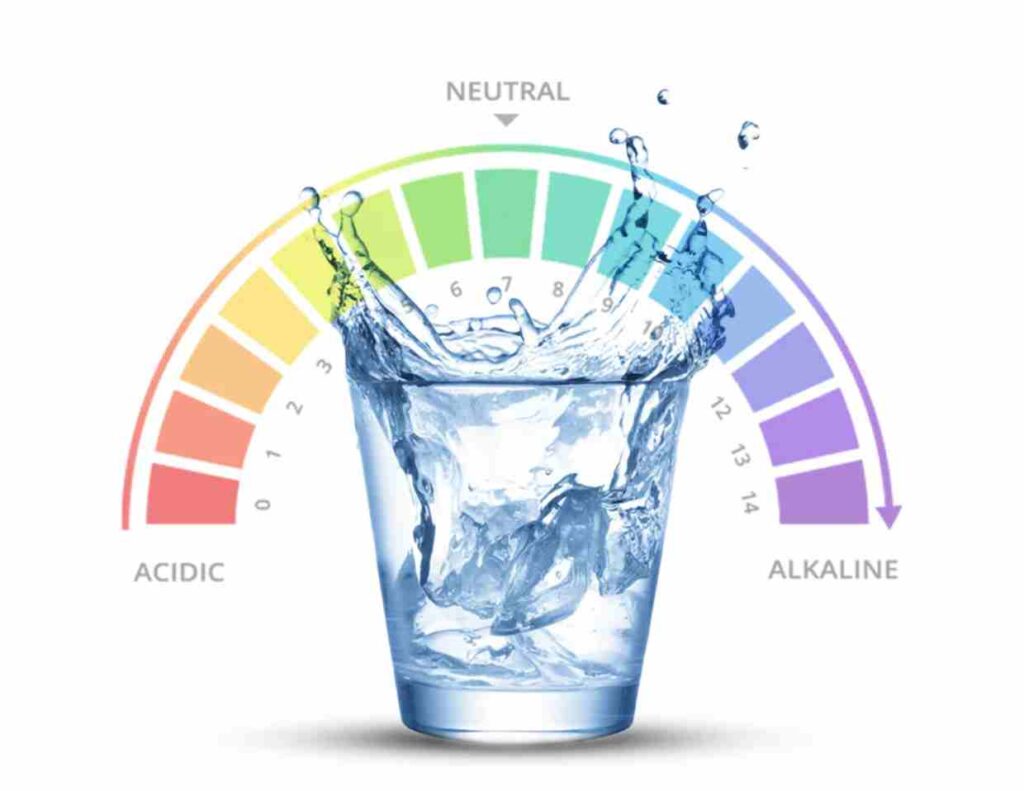
في الماء النقي، تركيز أيونات الهيدرونيوم يساوي تركيز أيونات الهيدروكسيد، وكلاهما يساوي 1.0 × 10⁻⁷ مول/لتر. هذا التعادل هو ما يحدد الرقم الهيدروجيني (pH) للماء النقي بقيمة 7.
موقع خان أكاديمي يقدم شرحاً ممتازاً لقيمة Kw وكيفية استخدامها.
مثال لتوضيح تأين الماء
لنفكر في الماء النقي عند درجة حرارة 25 درجة مئوية. تركيز أيونات H₃O⁺ هو 10⁻⁷ مول/لتر. هذا يعني أنه في لتر واحد من الماء، هناك فقط 0.0000001 مول من أيونات الهيدرونيوم! المليارات من جزيئات الماء الأخرى تبقى على حالها. هذا التركيز الضئيل هو ما يجعل الماء النقي ضعيف التوصيل للكهرباء، ولكنه كافٍ لجعله وسطاً للعديد من التفاعلات الحيوية.
إذا أضفنا حمضاً إلى الماء (مثل حمض الهيدروكلوريك)، فإن تركيز أيونات الهيدرونيوم H₃O⁺ يزداد. للحفاظ على قيمة Kw ثابتة (عند درجة حرارة ثابتة)، يجب أن ينخفض تركيز أيونات الهيدروكسيد OH⁻ تلقائياً. هذا هو السبب في أن المحاليل الحمضية تحتوي على أيونات هيدروكسيد أقل من المحاليل القاعدية.
لماذا يعتبر تأين الماء مهماً في جسم الإنسان؟
قد تظن أن تأين الماء مجرد تفصيل أكاديمي، لكنه حيوي لوجودك! إليك السبب:
- تنظيم درجة الحموضة في الدم (pH): دم الإنسان يحتاج إلى بقاء الرقم الهيدروجيني ضمن نطاق ضيق جداً (7.35-7.45). يعتمد الجسم على توازن أيونات H₃O⁺ و OH⁻ لتحقيق ذلك. أي خلل بسيط في هذا التوازن (الحماض أو القلاء) يمكن أن يكون قاتلاً.
- وظيفة الإنزيمات: جميع الإنزيمات في جسمك (التي تسرع التفاعلات الكيميائية) تعمل فقط ضمن نطاق pH محدد. تغير بسيط في تركيز أيونات الهيدرونيوم يمكن أن يعطل إنزيمات الهضم أو إنتاج الطاقة.
- نقل الإشارات العصبية: يعتمد عمل الخلايا العصبية والعضلية على تدفق الأيونات (مثل الصوديوم والبوتاسيوم والكالسيوم)، وهذا التدفق حساس جداً لدرجة الحموضة المحيطة.
- وظائف الكلى والرئتين: تعمل الكلى والرئتين معاً لتنظيم مستويات الأحماض والقواعد في الجسم، وكل ذلك يرجع في جوهره إلى إدارة تركيز أيونات الهيدرونيوم والهيدروكسيد الناتجة عن تأين الماء.
بحث منشور على PubMed (NCBI) يؤكد الدور الحاسم لتوازن الماء والأيونات في الحفاظ على الاستتباب الخلوي والوقاية من الأمراض.
للتعمق أكثر في سلوك الجزيئات المشحونة، يمكنك قراءة مقالنا عن الأيون الموجب والسالب.
الأسئلة الشائعة
هل تأين الماء يحدث فقط في الماء النقي؟
نعم، ولكنه يحدث في جميع المحاليل المائية. وجود أحماض أو قواعد أخرى يغير تركيزات H₃O⁺ و OH⁻، لكن تفاعل تأين الماء نفسه يظل يحدث في الخلفية ويخضع لنفس ثابت التوازن Kw.
كيف تؤثر درجة الحرارة على تأين الماء و Kw؟
التفاعل ماص للحرارة (يتطلب طاقة)، لذلك عند رفع درجة الحرارة، يزداد تأين الماء. هذا يعني أن قيمة Kw تزداد، ويصبح الرقم الهيدروجيني (pH) للماء المتعادل أقل من 7 (على سبيل المثال، عند 50 درجة مئوية، pH = 6.6، لكن الماء لا يزال متعادلاً لأن [H₃O⁺] = [OH⁻]).
لماذا نستخدم Kw بدلاً من دراسة تفاعل التأين مباشرة؟
لأن قياس Kw أسهل بكثير من قياس ثوابت التوازن لكل حمض وقاعدة على حدة. يوفر Kw نقطة مرجعية ثابتة لدرجة حرارة معينة، مما يسمح للكيميائيين بحساب تركيز H₃O⁺ أو OH⁻ في أي محلول مائي بسهولة.
هل يمكن أن يتأين الماء في الحالة الصلبة (الثلج) أو الغازية (البخار)؟
يحدث التأين الذاتي بدرجة كبيرة جداً في الحالة السائلة فقط. في الحالة الصلبة (الثلج)، الجزيئات مقيدة الحركة، ويكاد التأين ينعدم. في الحالة الغازية (البخار)، الجزيئات متباعدة جداً بحيث لا يمكن أن يحدث تفاعل بينها بسهولة.
كيف يرتبط مفهوم Kw بالرقم الهيدروجيني pH؟
الرقم الهيدروجيني (pH) يعرف بأنه اللوغاريتم السالب لتركيز أيون الهيدرونيوم: pH = -log[H₃O⁺]. باستخدام قيمة Kw، يمكننا أيضاً إيجاد pKw = -log(Kw) = 14 عند 25°م. ومن هنا جاءت فكرة أن مجموع pH و pOH (حيث pOH = -log[OH⁻]) يساوي 14 للمحاليل المائية.




💬 التعليقات