قانون الكثافة في الكيمياء
- ما هي الكثافة؟ تعريف ومفهوم أساسي
- العوامل التي تعتمد عليها الكثافة
- 1. درجة الحرارة (Temperature)
- 2. الضغط (Pressure)
- 3. طبيعة المادة ونوعها
- 4. الشوائب والإضافات
- شذوذ الكثافة: عندما يكسر الماء القواعد
- التفسير العلمي لشذوذ الماء
- تطبيقات عملية لقانون الكثافة
- أسئلة شائعة حول قانون الكثافة
- ما الفرق بين الكثافة والوزن النوعي؟
- كيف تؤثر الملوحة على كثافة الماء؟
- لماذا يرتفع الهواء الساخن؟
- كيف نحسب كثافة خليط من مواد مختلفة؟
- هل للكثافة علاقة باللزوجة؟
هل تساءلت يومًا لماذا يطفو الجليد على سطح الماء بينما تغوص قطعة الحديد؟ أو لماذا يرتفع بالون الهيليوم إلى السماء بينما يسقط بالون الهواء العادي؟ الإجابة كلها تكمن في مفهوم بسيط لكنه عميق التأثير: قانون الكثافة في الكيمياء.
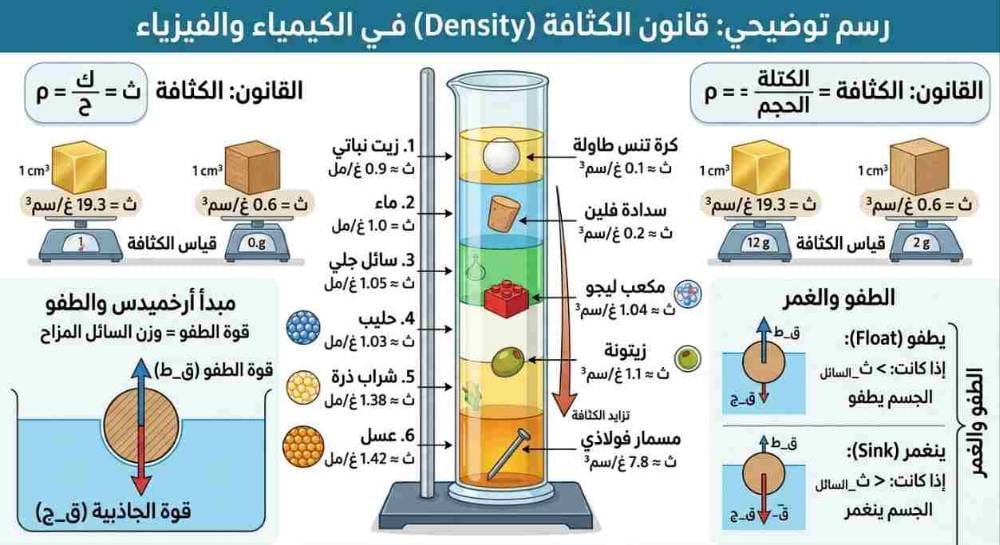
ما هي الكثافة؟ تعريف ومفهوم أساسي
الكثافة (Density) هي خاصية فيزيائية أساسية للمادة، تخبرنا بمدى “تراص” الجزيئات في وحدة الحجم. وفقًا لموسوعة بريتانيكا، تُعرف الكثافة بأنها “كتلة وحدة الحجم من المادة” . ببساطة، هي مقدار الكتلة الموجودة في حجم معين من المادة. تخيل صندوقين متساويين في الحجم، أحدهما مملوء بالريش والآخر بالحديد – صندوق الحديد أثقل بكثير لأن كثافته أعلى.
يمكن تعريف الكثافة رياضياً بالعلاقة البسيطة:
ρ = m / V
حيث ρ (الحرف اليوناني رو) هي الكثافة، m هي الكتلة، وV هو الحجم .
وحدات الكثافة تختلف حسب حالة المادة. للمواد الصلبة والسوائل، تُعبر عنها عادة بوحدة جرام/سنتيمتر مكعب (g/cm³) أو جرام/مليلتر (g/mL). أما الغازات فكثافتها أقل بكثير، لذلك تُعبر عنها بوحدة جرام/لتر (g/L) .
ما يميز الكثافة أنها خاصية مكثفة (Intensive Property)، أي أنها لا تعتمد على كمية المادة. قطعة صغيرة من الذهب لها نفس كثافة كتلة كبيرة منه. هذه الخاصية تجعل الكثافة أداة ممتازة للتعرف على المواد وتمييزها عن بعضها البعض.
العوامل التي تعتمد عليها الكثافة
الكثافة ليست قيمة ثابتة للمادة مهما تغيرت الظروف؛ بل تتأثر بعدة عوامل أساسية. فهم هذه العوامل يساعدنا في تفسير سلوك المواد في الطبيعة والصناعة.
1. درجة الحرارة (Temperature)
عندما ترتفع درجة حرارة المادة، تكتسب جزيئاتها طاقة حركية أكبر وتبتعد عن بعضها. هذا يؤدي إلى زيادة الحجم، وبما أن الكتلة ثابتة، فإن الكثافة تقل. هذه الظاهرة واضحة جدًا في الغازات، حيث الهواء الساخن أقل كثافة من الهواء البارد، مما يجعله يرتفع إلى الأعلى – وهو المبدأ الذي تعمل عليه البالونات والمناطيد.
العلاقة بين الكثافة ودرجة الحرارة تُعبر عنها بالمعادلة التقريبية:
ρ ∝ 1/T (عند ثبات الضغط)
2. الضغط (Pressure)
زيادة الضغط على المادة تضغط الجزيئات وتقربها من بعضها، مما يقلل الحجم ويزيد الكثافة. هذا التأثير واضح جدًا في الغازات، حيث العلاقة بين الكثافة والضغط طردية في ظروف درجة الحرارة الثابتة.
في الغازات المثالية، يمكننا اشتقاق معادلة دقيقة للكثافة من قانون الغاز المثالي (PV = nRT). بعد التعويض عن عدد المولات، نحصل على العلاقة:
ρ = (P × M) / (R × T)
حيث P الضغط، M الكتلة المولية، R ثابت الغازات العام (0.0821 L·atm/mol·K)، وT درجة الحرارة المطلقة بالكلفن. هذه المعادلة توضح أن كثافة الغاز تتناسب طردياً مع الضغط والكتلة المولية، وعكسياً مع درجة الحرارة المطلقة (Britannica – Density).
3. طبيعة المادة ونوعها
هذا العامل هو الأكثر وضوحًا. المواد المختلفة لها كثافات مختلفة بسبب الاختلاف في كتلة الذرات والمسافات بينها. على سبيل المثال:
- الذهب (Au): 19.3 g/cm³ – كثافته عالية بسبب كتلة ذراته الكبيرة.
- الألومنيوم (Al): 2.7 g/cm³ – كثافته منخفضة نسبياً لأنه معدن خفيف.
- الخشب: 0.4-0.8 g/cm³ – كثافته منخفضة بسبب المسافات الكبيرة بين جزيئاته.
4. الشوائب والإضافات
إضافة مواد أخرى إلى مادة نقية تغير كثافتها. فمثلاً، ماء البحر أكثر كثافة من الماء العذب بسبب الأملاح الذائبة فيه. هذه الخاصية تستخدم في العديد من التطبيقات الصناعية، مثل قياس تركيز المحاليل من خلال قياس كثافتها.
شذوذ الكثافة: عندما يكسر الماء القواعد
هنا يأتي الجزء الأكثر إثارة. معظم المواد تتصرف كما شرحنا: عندما تنخفض درجة الحرارة، تزداد كثافتها. لكن الماء النقي يفعل العكس في نطاق درجة حرارة معين! هذه الظاهرة تسمى شذوذ الكثافة (Anomalous Expansion of Water).
دعني أوضح لك بالأرقام. كثافة الماء عند 4°م هي 1.000 g/cm³. عندما تبرد الماء من 4°م إلى 0°م، تبدأ كثافته في الانخفاض بدلاً من الارتفاع! وعندما يتجمد الماء عند 0°م، يصبح كثافة الجليد 0.917 g/cm³ فقط، أي أقل من كثافة الماء السائل.
هذا الشذوذ هو السبب في:
- طفو الجليد على الماء: الأنهار والبحار تتجمد من السطح، وليس من القاع. لو كان الجليد أثقل من الماء، لغطس إلى القاع وتجمدت المسطحات المائية بأكملها!
- بقاء الحياة تحت الجليد: طبقة الجليد العائمة تعزل الماء تحتها، مما يحافظ على درجة حرارة مناسبة للكائنات الحية في الشتاء.
- تكسير الأنابيب: عندما يتجمد الماء داخل الأنابيب، يتمدد ويكسرها – وهو تحذير مهم لأصحاب المنازل في المناطق الباردة.
التفسير العلمي لشذوذ الماء
السر يكمن في التركيب الجزيئي للماء وجزيئات الهيدروجين. جزيء الماء (H₂O) له شكل منحني بزاوية 104.5 درجة، ويشكل روابط هيدروجينية مع الجزيئات المجاورة. عند التبريد إلى 4°م، تتقارب الجزيئات وتزداد الكثافة. لكن عند التبريد إلى ما دون 4°م، تبدأ الروابط الهيدروجينية في ترتيب الجزيئات في بنية بلورية سداسية تحتوي على فراغات كبيرة، مما يزيد الحجم ويقلل الكثافة. هذه البنية تتشكل بشكل كامل عند التجمد، مما يعطي الجليد كثافة أقل .
الماء هو المادة الوحيدة المعروفة التي تتمدد عند التجمد بدلاً من الانكماش، وهذه الخاصية الفريدة كانت حاسمة لنشوء الحياة على الأرض.
تطبيقات عملية لقانون الكثافة
فهم قانون الكثافة في الكيمياء له تطبيقات واسعة في حياتنا اليومية والصناعة:
- الكشف عن غش الذهب: قياس كثافة الذهب تكشف إذا كان ممزوجاً بمعادن أخف.
- صناعة السفن: السفن الضخمة المصنوعة من الفولاذ تطفو لأن تصميمها يجعل متوسط كثافتها (مع الهواء المحبوس داخلها) أقل من كثافة الماء.
- أجهزة قياس كثافة البول: تستخدم في المختبرات الطبية للكشف عن أمراض الكلى والسكري.
- الصناعات الغذائية: قياس كثافة الحليب يكشف عن غشه بالماء.
- صناعة البطاريات: قياس كثافة حمض الكبريتيك في بطاريات السيارات يحدد مستوى الشحن.
أسئلة شائعة حول قانون الكثافة
ما الفرق بين الكثافة والوزن النوعي؟
الكثافة هي الكتلة لكل وحدة حجم (وحدة: g/cm³). أما الوزن النوعي (Specific Gravity) فهو نسبة كثافة المادة إلى كثافة الماء عند 4°م، وهو كمية بلا وحدات. الوزن النوعي مفيد لأنه لا يتغير بتغير وحدات القياس.
كيف تؤثر الملوحة على كثافة الماء؟
إضافة الأملاح تزيد كثافة الماء. كثافة ماء البحر المتوسط حوالي 1.027-1.030 g/cm³، بينما ماء البحر الميت شديد الملوحة تصل كثافته إلى 1.24 g/cm³، مما يسمح للإنسان بالطفو بسهولة دون جهد.
لماذا يرتفع الهواء الساخن؟
الهواء الساخن أقل كثافة من الهواء البارد المحيط به، لذلك يخضع لقوة الطفو التي تدفعه إلى الأعلى. هذا المبدأ هو أساس عمل البالونات والمناطيد.
كيف نحسب كثافة خليط من مواد مختلفة؟
إذا كان الخليط متجانساً، نقسم الكتلة الكلية على الحجم الكلي. لكن الخلائط غير المتجانسة (مثل الزيت والماء) لا يمكن حساب كثافتها بهذه الطريقة لأنها لا تمتزج – هنا نفكر في كثافة كل طبقة على حدة.
هل للكثافة علاقة باللزوجة؟
لا توجد علاقة مباشرة بين الكثافة واللزوجة. الزئبق مثلاً كثافته عالية جداً لكن لزوجته منخفضة، بينما العسل كثافته أقل بكثير لكن لزوجته عالية جداً. اللزوجة تعتمد على قوى الاحتكاك بين الجزيئات وليس على كتلتها فقط.
أتمنى أن تكون هذه الرحلة في عالم الكثافة قد أضافت لك منظوراً جديداً لهذا المفهوم البسيط لكن العميق. تذكر أن الكثافة ليست مجرد رقم في كتاب؛ إنها تفسر لماذا تطفو الجبال الجليدية، ولماذا نستطيع السباحة في البحر الميت، ولماذا تشتغل بالونات الهواء الساخن. إذا كان لديك سؤال أو تجربة مثيرة في التعامل مع الكثافة، شاركها في التعليقات.
كما يمكنك الاطلاع على مقالنا السابق عن قانون النسب الثابتة في الكيمياء لفهم كيف تخضع المركبات الكيميائية لقوانين دقيقة.




💬 التعليقات