قانون النسب المتضاعفة: تعريفها ، امثلة ، تاريخها
- ما هي النسب المتضاعفة في الكيمياء؟
- قانون النسب المتضاعفة: التعريف والتاريخ
- أمثلة على قانون النسب المتضاعفة محللة خطوة بخطوة
- المثال الأول: أكاسيد النيتروجين (الأكثر شهرة)
- المثال الثاني: أكاسيد الكربون (الأقرب للحياة اليومية)
- المثال الثالث: مركبات الكبريت مع الأكسجين (تطبيق عملي)
- كيف تحل مسائل قانون النسب المتضاعفة؟ دليل عملي
- لماذا يظل قانون النسب المتضاعفة ذا صلة حتى اليوم؟
- الأسئلة الشائعة حول قانون النسب المتضاعفة
- ما هو قانون النسب المتضاعفة باختصار؟
- من هو العالم الذي صاغ قانون النسب المتضاعفة؟
- ما الفرق بين قانون النسب المتضاعفة وقانون النسب الثابتة؟
- كيف أطبق قانون النسب المتضاعفة في المسائل الكيميائية؟
- لماذا يعتبر قانون النسب المتضاعفة أساسياً في الكيمياء الحديثة؟
تخيل أنك تمسك بقطعتين من العجين، وتبدأ في تشكيلهما بنسب مختلفة: مرة تضع ملعقة سكر لكل كوب دقيق، ومرة تضع ملعقتين. النتيجة؟ حلويتان مختلفتان تماماً في المذاق والقوام. هذا المبدأ البسيط هو جوهر قانون النسب المتضاعفة في الكيمياء، لكن بدلاً من العجين والسكر، نتحدث عن ذرات وعناصر حقيقية تحكم عالمنا المادي.
كمدرس كيمياء قضيت سنوات أشرح هذا المفهوم للطلاب، لاحظت أن الفهم الحقيقي يأتي عندما نربط القانون المجرد بأمثلة من الحياة. اليوم، سأصحبك في رحلة مبسطة لاكتشاف أحد أركان الكيمياء الحديثة، مع أمثلة محللة خطوة بخطوة ستجعلك تقول: “آه، الآن فهمت!”
ما هي النسب المتضاعفة في الكيمياء؟
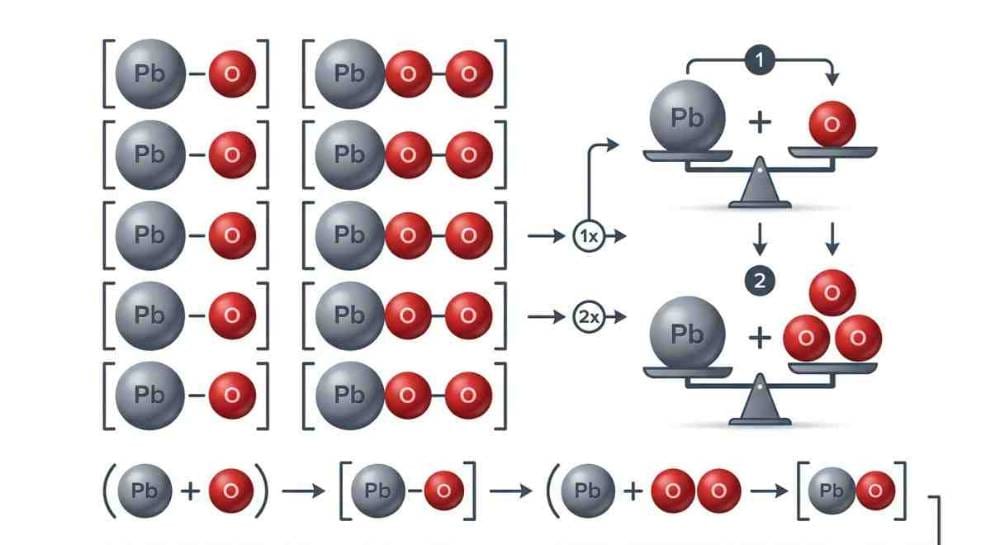
قبل أن نغوص في صلب القانون، دعنا نوضح فكرة النسب المتضاعفة بلغة يومية. عندما يتحد عنصران كيميائيان (مثل الكربون والأكسجين) لتكوين مركب، فإنهما لا يفعلان ذلك بنسب عشوائية. بل تتحد ذراتهما بنسب محددة وثابتة.
المثير للاهتمام يحدث عندما نكتشف أن نفس العنصرين يمكنهما تكوين أكثر من مركب. هنا تظهر النسب المتضاعفة: كتل أحد العنصرين التي تتحد مع كتلة ثابتة من العنصر الآخر تكون في علاقة أعداد صحيحة بسيطة (1:2، 2:3، 1:3، وهكذا).
لماذا الأعداد الصحيحة؟ لأن الذرات وحدات منفصلة لا تتجزأ في التفاعلات الكيميائية العادية. لا يمكن أن تتحد “نصف ذرة” مع ذرة أخرى، ولهذا تأتي النسب دائماً على شكل أرقام صحيحة. هذه الفكرة البسيطة غيرت مسار العلم للأبد.
قانون النسب المتضاعفة: التعريف والتاريخ
صاغ العالم البريطاني جون دالتون هذا القانون عام 1803، بعد سنوات من المراقبة الدقيقة لتفاعلات الغازات. لاحظ دالتون أن النيتروجين والأكسجين يتحدان لتكوين عدة مركبات (مثل NO، NO₂، N₂O)، وأن كتل الأكسجين المتحدة مع كتلة ثابتة من النيتروجين كانت دائماً في نسب بسيطة: 1:2:3:4:5.
“إذا اتحد عنصران لتكوين أكثر من مركب، فإن الكتل المختلفة من أحد العنصرين التي تتحد مع كتلة ثابتة من العنصر الآخر، تكون في نسبة أعداد صحيحة بسيطة.”
لم يكن دالتون يعرف حينها أن الذرات هي الوحدات الأساسية، لكن ملاحظاته التجريبية قادت إلى استنتاج ثوري: المادة مكونة من جسيمات منفصلة. هذا القانون، مع قانون النسب الثابتة لبروست، شكل الدعامتين اللتين بنى عليهما دالتون نظريته الذرية الشهيرة.
الأهمية التاريخية لا تقل عن العلمية: قبل دالتون، كانت الكيمياء تعتمد على الوصف النوعي. بعد قانون النسب المتضاعفة، أصبح بالإمكان التنبؤ بتكون المركبات وحساب نسبها بدقة رياضية. لمزيد من التفاصيل التاريخية الموثقة، يمكنك الرجوع لمصدر موثوق مثل موسوعة بريتانيكا.
أمثلة على قانون النسب المتضاعفة محللة خطوة بخطوة
النظرية جميلة، لكن التطبيق هو ما يثبت الفهم. إليك ثلاثة أمثلة كلاسيكية، سأشرحها كما أشرحها لطلابي في المختبر:
المثال الأول: أكاسيد النيتروجين (الأكثر شهرة)
يتحد النيتروجين (N) مع الأكسجين (O) لتكوين خمسة مركبات مختلفة. لنثبت كتلة النيتروجين عند 14 جرام (الكتلة المولية تقريباً)، ونرى كم جراماً من الأكسجين يتحد معها في كل مركب:
- N₂O: 14 جم نيتروجين + 8 جم أكسجين
- NO: 14 جم نيتروجين + 16 جم أكسجين
- N₂O₃: 14 جم نيتروجين + 24 جم أكسجين
- NO₂: 14 جم نيتروجين + 32 جم أكسجين
- N₂O₅: 14 جم نيتروجين + 40 جم أكسجين
الآن، لنقسم كتل الأكسجين على أصغر قيمة (8 جم):
- 8 ÷ 8 = 1
- 16 ÷ 8 = 2
- 24 ÷ 8 = 3
- 32 ÷ 8 = 4
- 40 ÷ 8 = 5
النسبة النهائية: 1 : 2 : 3 : 4 : 5 ← أعداد صحيحة بسيطة تماماً! هذا هو قانون النسب المتضاعفة في أبهى صوره.
المثال الثاني: أكاسيد الكربون (الأقرب للحياة اليومية)
الكربون والأكسجين يتحدان لتكوين مركبين رئيسيين نصادفهما يومياً:
- أول أكسيد الكربون (CO): 12 جم كربون + 16 جم أكسجين
- ثاني أكسيد الكربون (CO₂): 12 جم كربون + 32 جم أكسجين
بثبات كتلة الكربون (12 جم)، نقارن كتل الأكسجين: 16 جم و 32 جم. النسبة بينهما: 16:32 = 1:2. بسيطة وواضحة!
هذا المثال يفسر لماذا ينتج احتراق الوقود غير الكامل غاز CO السام، بينما ينتج الاحتراق الكامل CO₂ الأقل خطورة. الفرق في نسبة الأكسجين يغير كل شيء.
المثال الثالث: مركبات الكبريت مع الأكسجين (تطبيق عملي)
لنخرج عن المألوف قليلاً. الكبريت (S) يتحد مع الأكسجين لتكوين:
- ثاني أكسيد الكبريت (SO₂): 32 جم كبريت + 32 جم أكسجين
- ثالث أكسيد الكبريت (SO₃): 32 جم كبريت + 48 جم أكسجين
نسبة الأكسجين: 32 : 48 = 2 : 3 بعد التبسيط. مرة أخرى، أعداد صحيحة بسيطة تؤكد القانون.
هذا المثال مهم صناعياً، لأن SO₂ و SO₃ يدخلان في إنتاج حمض الكبريتيك، أحد أهم المواد الكيميائية في العالم. فهم النسب يساعد المهندسين على تحسين الإنتاج وتقليل الهدر.
كيف تحل مسائل قانون النسب المتضاعفة؟ دليل عملي
كثير من الطلاب يحفظون القانون لكن يتعثرون في التطبيق. إليك طريقتي المكونة من 4 خطوات التي جعلت عشرات طلابي يتقنون المسائل:
- ثبّت كتلة أحد العنصرين: اختر العنصر الأسهل في الحساب (غالباً ذو الكتلة المولية الأصغر) واجعل كتلته ثابتة في جميع المركبات.
- احسب كتل العنصر الآخر: لكل مركب، احسب كتلة العنصر الثاني التي تتحد مع الكتلة الثابتة التي اخترتها.
- استخرج النسبة: اقسم الكتل التي حصلت عليها على أصغر قيمة بينها، أو على عامل مشترك لتبسيطها.
- بسّط لأبسط أعداد صحيحة: النتيجة النهائية يجب أن تكون نسباً مثل 1:2، 2:3، 3:4، إلخ. إذا ظهرت كسور، اضرب جميع الأطراف في رقم يجعلها صحيحة.
نصيحة من خبير: دائماً راجع حساباتك بالكتل المولية من الجدول الدوري. خطأ بسيط في الكتلة الذرية قد يقلب النسبة رأساً على عقب. وإذا احترت، ابدأ بمثال النيتروجين والأكسجين كمرجع ذهني.
لماذا يظل قانون النسب المتضاعفة ذا صلة حتى اليوم؟
قد يتساءل البعض: “هذا القانون من القرن التاسع عشر، ما فائدته في عصر الكيمياء الحاسوبية والنانو؟” الإجابة: أكثر مما تتخيل.
أولاً، القانون يعلمنا التفكير النسبي في الكيمياء. قبل أن تحسب أي شيء، اسأل: “ما النسبة المنطقية بين المكونات؟” هذا المنهج يوفر وقتاً ويقلل الأخطاء في المختبر والصناعة.
ثانياً، فهم النسب المتضاعفة أساسي في مجالات مثل الكيمياء التحليلية و هندسة المواد. عندما تصمم سبيكة جديدة أو تحلل عينة مجهولة، تعتمد على مبادئ دالتون لتحديد التركيب.
ثالثاً، القانون يذكرنا بقيمة الملاحظة الدقيقة. دالتون لم يكن يملك أجهزة متطورة، لكن صبره ودقته غيّرا العلم. في عصرنا، حيث نعتمد على البرامج الجاهزة، هذه الدرس لا يزال ذهبياً.
للاطلاع على مناقشات متعمقة حول دلالات الأعداد الصحيحة في القانون، أنصح بزيارة هذا النقاش المتخصص على Chemistry Stack Exchange.
الأسئلة الشائعة حول قانون النسب المتضاعفة
ما هو قانون النسب المتضاعفة باختصار؟
ينص قانون النسب المتضاعفة على أنه عندما يتحد عنصران لتكوين أكثر من مركب، فإن كتل أحد العنصرين التي تتحد مع كتلة ثابتة من العنصر الآخر تكون في نسبة أعداد صحيحة بسيطة. اكتشفه جون دالتون عام 1803 ويُعد حجر أساس في النظرية الذرية.
من هو العالم الذي صاغ قانون النسب المتضاعفة؟
العالم البريطاني جون دالتون هو من صاغ قانون النسب المتضاعفة عام 1803، استناداً إلى ملاحظاته الدقيقة لتفاعلات الغازات ومركبات الأكسجين مع النيتروجين والكربون.
ما الفرق بين قانون النسب المتضاعفة وقانون النسب الثابتة؟
قانون النسب الثابتة (بروست) ينطبق على مركب واحد فقط، حيث تكون نسبة العناصر فيه ثابتة دائماً. أما قانون النسب المتضاعفة (دالتون) فيقارن بين مركبين أو أكثر يتكونان من نفس العنصرين، وتكون نسب الكتلة بينهما أعداداً صحيحة بسيطة.
كيف أطبق قانون النسب المتضاعفة في المسائل الكيميائية؟
لحل مسائل القانون: 1) ثبّت كتلة أحد العنصرين في جميع المركبات، 2) احسب كتل العنصر الآخر المقترنة بها، 3) اقسم الكتل على بعضها لاستخراج النسبة، 4) بسّط النتيجة لأبسط أعداد صحيحة. المثال الكلاسيكي: أكاسيد النيتروجين تعطي نسباً مثل 1:2:3:4:5.
لماذا يعتبر قانون النسب المتضاعفة أساسياً في الكيمياء الحديثة؟
بسبب أنه قدّم أول دليل تجريبي مقنع على وجود الذرات كوحدات منفصلة غير قابلة للتجزئة، وساعد دالتون في بناء نظريته الذرية التي شكلت حجر الأساس للكيمياء الحديثة وفهمنا للتركيب الجزيئي.
وصلنا لنهاية الرحلة، لكن التعلم لا يتوقف. إذا جربت حل مسألة باستخدام القانون وواجهت صعوبة، أو لديك مثال آخر تود مشاركته، اترك تعليقاً أسفل المقال. يسعدني جداً أن أتفاعل معكم وأجيب على استفساراتكم.
المراجع والمصادر الموثوقة:
– Britannica, Law of Multiple Proportions: https://www.britannica.com/science/law-of-multiple-proportions
– Study.com, Lesson Examples: https://study.com/academy/lesson/law-of-multiple-proportions-definition-examples.html
– Chemistry Stack Exchange, Significance of Whole Numbers: https://chemistry.stackexchange.com/questions/3975/




💬 التعليقات